 |
|
Популярные авторы:: Толстой Лев Николаевич :: Горький Максим :: Чехов Антон Павлович :: Грин Александр :: Борхес Хорхе Луис :: Азимов Айзек :: Раззаков Федор :: Херберт Фрэнк :: БСЭ :: Картленд Барбара Популярные книги:: Дюна (Книги 1-3) :: Алешкино сердце :: Вялiкае сэрца (на белорусском языке) :: Дождь, которому хотелось курить :: Асунта :: The Boarding House :: Биннор :: Я тебя люблю, и я тебя тоже нет :: Домашние животные :: Оправдание «Бувара и Пекюше» |
Большая Советская Энциклопедия (ЭЛ)ModernLib.Net / Энциклопедии / БСЭ / Большая Советская Энциклопедия (ЭЛ) - Чтение (стр. 11)
Форма зубцов в разных отведениях в общем различна. Сравнимость ЭКГ у разных лиц достигается стандартными условиями регистрации: способом наложения электродов на кожу конечностей и грудной клетки (обычно используется 12 отведений), определёнными чувствительностью аппарата (1
мм =0,1
мв) и скоростью движения бумаги (25 или 50
ммв сек); исследуемый, как правило, находится в положении лёжа, в условиях покоя (при специальных показаниях - и после физической, лекарственной или другие нагрузки). При анализе ЭКГ оценивают наличие, величину, форму и ширину зубцов и интервалов между ними и на этом основании судят об особенностях электрических процессов в сердце в целом и в некоторой степени - об электрической активности более ограниченных участков сердечной мышцы.
В медицине Э. имеет наибольшее значение для распознавания нарушений сердечного ритма, а также для выявления инфаркта миокарда и некоторых других заболеваний. Однако изменения ЭКГ отражают лишь характер нарушения электрических процессов и, как правило, не являются строго специфичными для определённой болезни. Изменения ЭКГ могут возникать не только в результате заболевания, но и под влиянием обычной дневной активности, приёма пищи, лекарственного лечения и других причин. Поэтому диагноз ставится врачом не по ЭКГ, а по совокупности клинико-лабораторных признаков заболевания. Диагностические возможности возрастают при сопоставлении ряда последовательно снятых ЭКГ (с интервалом в несколько дней или недель). Электрокардиограф используется также в кардиомониторах (аппаратах круглосуточного автоматического наблюдения за состоянием тяжелобольных) и для телеметрического контроля за состоянием работающего человека - в клинической, спортивной, космической медицине, что обеспечивается специальными способами наложения электродов и радиосвязью между гальванометром и регистрирующим устройством. Биоэлектрическая активность сердца может быть зарегистрирована и другим способом. Разность потенциалов характеризуется определёнными для данного момента величиной и направлением, т. е. является и может быть условно представлена стрелкой, занимающей определенное положение в пространстве. Характеристики этого вектора изменяются в течение сердечного цикла так, что его начальная точка остаётся неподвижной («электрический центр сердца»), а конечная - описывает сложную замкнутую кривую. В проекции на плоскость эта кривая имеет вид серии петель и называется векторкардиограммой (ВКГ); приближённо она может быть построена графически на основании ЭКГ в разных отведениях, но её можно получить и непосредственно при помощи специального аппарата - векторкардиографа, в котором регистрирующим устройством является катодно-лучевая трубка, а для отведения используются 2 пары электродов, размещенных на обследуемом в соответствующей плоскости. Меняя положение электродов, можно получить ВКГ в различных плоскостях и составить более полное пространственное представление о характере электрических процессов. В некоторых случаях векторкардиография дополняет Э. как диагностический метод. Изучение электрофизиологических основ и клинического применения Э. и векторкардиографии, совершенствование аппаратов и методов регистрации - предмет особого научного раздела медицины - электрокардиологии. В ветеринарии Э. применяется у крупных и мелких животных (в основном у лошадей, крупного рогатого скота, собак) для диагностики изменений в сердце, возникающих в результате некоторых незаразных или инфекционных болезней. С помощью Э. у животных определяют нарушения сердечного ритма, увеличение отделов сердца (предсердий, желудочков) и другие изменения в сердце. Э. позволяет контролировать действие на сердечную мышцу животного применяемых или испытываемых лекарственных средств. Лит.:Исаков И. И., Кушаковский М. С., Журавлева Н. Б., Клиническая электрокардиография, Л., 1974; Сумароков А. В., Михайлов А. А., Клиническая электрокардиография, 3 изд., М., 1975; Friedman Н. Н., Diagnostic electrocardiography and vectorcardiography, N. Y., 1971; Chung Е. К., Electrocardiography. Practical applications with vectorial principles, N. Y., 1974. А. А. Михайлов. 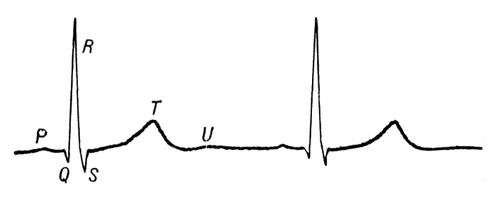
Нормальная кардиограмма. Электрокатализ Электроката'лиз,изменение скорости и селективности электрохимических реакций, достигаемое в результате каталитического действия электродов, на поверхности которых эти реакции протекают. Явление Э. впервые было обнаружено в начале 20 в., когда в ряде работ была установлена зависимость скорости катодного выделения водорода от материала электрода. Широкое распространение Э. получил только после 1960, главным образом в связи с развитием исследований, связанных с проблемой .Э. тесно связан с адсорбцией реагирующих, промежуточных и конечных продуктов реакции. Основным вопросом теории Э. является выяснение природы и предсказание каталитической активности различных электродных материалов. Иногда понятие Э. связывают также с изучением адсорбционных и других физико-химических свойств поверхности различных катализаторов электрохимическими методами, а также с изучением кинетики и механизма электрохимических стадий в каталитических процессах в растворах - жидкофазного восстановления или окисления. В ряде случаев эти процессы сводятся к сопряжённым электрохимическим реакциям, например катодного восстановления гидрируемого вещества и анодного окисления водорода. Э. имеет большое значение для повышения эффективности работы и .Во многих случаях в этих устройствах с целью ускорения электрохимических процессов используются электроды, покрытые платиновыми катализаторами. Одна из практически важных задач исследований в области Э. - разработка менее дорогих и менее дефицитных катализаторов - металлических и неметаллических материалов с высокой электрокаталитической активностью (в т. ч. окислов, органических полупроводников и др.). В. С. Багоцкий. 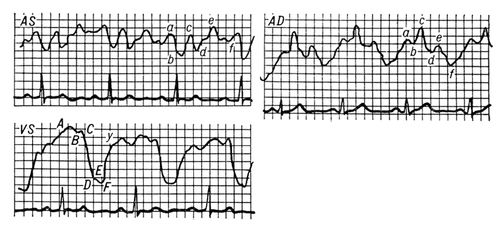
Электрокимограмма здорового человека: AS - левого предсердия; AD - правого предсердия; VS - левого желудочка; латинскими буквами обозначены отдельные элементы кривых. Электрокаустика Электрока'устика(от и греч. kaustikos - жгучий), то же, что . Электрокимография Электрокимогра'фия(от ,греч. kyma - волна и ), графический метод исследования сердечно-сосудистой системы при помощи рентгенодиагностической аппаратуры и электрокимографа (см. ) .Предложена немецким врачом К. Хекманом в 1936. Рентгеновские лучи, пройдя через определённый участок тела исследуемого и щель специальной камеры, попадают на экран фотоэлемента. Возникающий в цепи фотоэлемента электрический ток передаётся на электронный усилитель. Если в фотоэлемент попадают лучи, проходящие через пульсирующий контур сердца или сосуда, то возникающий ток меняется соответственно пульсации исследуемого органа; изменения тока записываются в виде кривой - электрокимограммы. В случае, когда фотоэлемент расположен непосредственно за пульсирующим органом, электрокимограмма отразит разницу в кровенаполнении этого органа во время и .Отклонения формы электрокимограмм от характерных для определённых отделов сердца ( рис. ) и крупных сосудов, а также изменения протяжённости отдельных отрезков кривой могут иметь диагностическое значение. Э. применяется главным образом для распознавания аневризм, некоторых пороков сердца, перикардитов и других заболеваний сердца и сосудов, а также в клинической фармакологии и физиологии. Лит.:3арецкий В. В., Электрокимография, М., 1963; Орлов В. Н., Электрокимография в клинике внутренних болезней, М., 1964. Л. Л. Орлов. Электрокинетические явления Электрокинети'ческие явле'ния,группа явлений, наблюдаемых в дисперсных системах и капиллярах и выражающихся либо в возникновении движения одной из фаз по отношению к другой под действием внешнего электрического поля ( , ) ,либо в возникновении разности потенциалов в направлении относительного движения фаз, вызываемого механическими силами (седиментационный потенциал, или эффект Дорна, потенциал течения). Э. я. обусловлены существованием на границе фаз избыточных зарядов, располагающихся в виде двух противоположно заряженных слоев, называемых .Внешнее электрическое поле, направленное вдоль границы фаз, вызывает смещение одного ионного слоя по отношению к другому, что приводит к относительному перемещению фаз, т. е. к электроосмосу или электрофорезу. Аналогичным образом при течении жидкости или оседании частиц дисперсной фазы наблюдаются явления, обратные электроосмосу и электрофорезу, - относительное движение ионных слоев и пространственное разделение зарядов (поляризация) в направлении движения фаз, т. е. возникновение соответственно потенциалов течения или седиментации. Любое из Э. я. может быть использовано для определения x. При этом учитывают, что поверхностная проводимость, обусловленная подвижными зарядами двойного электрического слоя, превышает объёмную проводимость системы. Теория Э. я., разработанная М. (1903), устанавливает линейную зависимость между количеств, характеристиками Э. я. и внешнего электрического поля. В этой теории, однако, не учитывается отклонение двойного электрического слоя от равновесия и возникновение у дисперсных частиц индуцированного дипольного момента. Для учёта этого явления необходимо исследовать Э. я. совместно с другими электроповерхностными явлениями. Лит.:Духин С. С., Электропроводность и электрокинетические свойства дисперсных систем, К., 1975; Духин С. С., Дерягин Б. В., Электрофорез, М., 1976. С. С. Духин. Электрокинетический потенциал Электрокинети'ческий потенциа'л,x-потенциал, дзета-потенциал, часть общего скачка потенциала на границе двух фаз, определяющая относительное перемещение этих фаз при .Общий скачок потенциала при пересечении межфазной границы в дисперсных системах обусловлен существованием .Э. п. - перепад потенциала по той части диффузного слоя, в пределах которой жидкость может быть вовлечена в тангенциальное движение относительно межфазной поверхности при внешнем воздействии на систему. Под влиянием сильно адсорбирующихся на поверхности ионов или изменения pH жидкости может произойти перемена знака на противоположный («перезарядка» поверхности). Э. п. в равен нулю. Электрокоагуляция Электрокоагуляция(от и ) ,образование агрегатов частиц дисперсной фазы под воздействием внешнего электрического поля (см. также ) .Э. обусловлена тем, что внешнее электрическое поле деформирует (поляризует) двойной электрический слой, существующий вблизи поверхности частиц дисперсной фазы. См. также . Электроконтактный телеграфный регулятор Электроконта'ктный телегра'фный регуля'тор, ,предназначенный для поддержания номинальной частоты вращения вала электродвигателя в приводе электромеханического с целью уменьшения искажений при передаче телеграфных сигналов. Электрокоптильная установка Электрокопти'льная устано'вка,см. в ст. . Электрокопчение Электрокопче'ние,способ ,при котором тепловая обработка рыбных или мясных продуктов осуществляется с помощью инфракрасного излучения, а осаждение дыма на продукт происходит в электрическом поле при коронном разряде (электрическое поле, воздействуя на ионизированные частицы дыма, вызывает его ускоренное осаждение на продукт). Э. позволяет сократить продолжительность копчения, полностью механизировать и автоматизировать производство, повысить коэффициент использования дыма. Одновременно при Э. уменьшаются технологические потери на 6-12%, снижаются трудоёмкость процесса, а также себестоимость продукции при её высоком качестве. Электрокорунд Электрокору'нд,искусственный абразивный материал, в состав которого входят преимущественно закристаллизованный глинозём ( ) в форме a-фазы ( ) ,а также окислы кремния, титана, кальция и железа. Получают плавкой глинозёмсодержащего сырья в дуговых печах с последующей кристаллизацией расплава. Плотность Э. (кроме сферокорунда) 3,9-4,0 г/см 3 ,микротвёрдость 19-24 Гн/м 2 .В зависимости от содержания глинозёма и особенностей технологии плавки различают несколько разновидностей Э. Нормальный Э.,состоящий из корунда (до 95%) с небольшой примесью шлаков и ферросплава, широко используется для обработки металлов. Белый Э. получают путём переплава чистой окиси алюминия (g-фазы). Содержит 98-99% корунда и сравнительно мало примесей. По свойствам и химическому составу белый Э. более однороден, чем нормальный. Микротвёрдость его несколько выше, чем у нормального Э. Применяется для обработки высокопрочных сплавов, при скоростном и прецизионном шлифовании. Легированный Э. (хромистый, титанистый, циркониевый) имеет свойства, зависящие от состава и содержания примесных элементов. из легированного Э. применяются для обработки деталей из конструкционных и некоторых инструментальных сталей. Монокорунд, состоящий из плоскогранных изометричных зёрен монокристаллического корунда с небольшим содержанием примесей (2-3%), получают путём сплавления боксита с сернистым железом. Абразивные инструменты из монокорунда используются для шлифования труднообрабатываемых жаропрочных, конструкционных и других легированных сталей и сплавов. Сферокорунд получают из глинозёма в виде полых корундовых сфер (плотность его 2,2 г/ см 3) ;содержит небольшое (<1%) количество примесей. Абразивные инструменты из сферокорунда применяют для обработки мягких и вязких материалов (цветных металлов, пластмасс, резины, кожи). Электрокорундовые зёрна, порошки и микропорошки составляют около 80% общего объёма производства абразивных материалов. Благодаря высокой огнеупорности, стойкости в кислотах и щелочах, хорошей теплопроводности, малому термическому расширению и низкой электропроводности Э. широко применяется также для изготовления огнеупорных, химически инертных изделий, керамических деталей электровакуумных приборов, изоляторов и т. д. Э. используют и как наполнитель в жароупорных бетонах и массах для набивки тиглей индукционных печей. Значительное количество Э. потребляет чёрная металлургия (получение синтетических шлаков для рафинирования жидкой стали). Области использования Э. непрерывно расширяются. Лит.:Производство абразивных материалов, Л., 1968; Рысс М. А., Производство металлургического электрокорунда, М., 1971; Абразивные материалы и инструменты. Каталог-справочник, М., 1976. М. Л. Мейльман. Электрокристаллизация Электрокристаллиза'ция,электроосаждение, кристаллизация металлов и сплавов на катоде при электролизе растворов и расплавов соответствующих солей. Рост кристаллов при Э. металлов имеет много общего с из пара или раствора, фактором, определяющим пересыщение при Э., является ,возникающее на электроде в ходе электрохимической реакции. В зависимости от величины перенапряжения рост кристаллов может происходить путём спирально-слоевого роста на винтовых ,образования и разрастания двумерных зародышей (особенно на бездислокационных кристаллах) и при достаточно высоких пересыщениях - путём образования трёхмерных зародышей или нормального роста кристаллов. Возможность изменения перенапряжения на катоде в широких пределах позволяет при Э. получать слои металлов с сильно различающимися свойствами. Так, в зависимости от условий образования осадков плотность дислокаций в них может изменяться от 10 6до 10 12 см -2 ,соответственно изменяются и такие свойства, как электропроводность, твёрдость, пластичность. Высокие плотности дислокаций были обнаружены в осадках меди, никеля, железа, хрома, платины, серебра и др. Особенно сильное влияние на структуру осадков металлов, полученных методом Э., оказывает адсорбция и включение примесей. Э. лежит в основе , металлов, . Ю. М. Полукаров. Электролечение Электролече'ние,электротерапия, лечение электрическими токами и электромагнитными полями. При Э. применяют постоянный ток низкого напряжения (см. ) ,переменные токи (см. , ) , в том числеимпульсные токи низкой частоты (см. ) ,постоянное электрическое поле высокой напряжённости (см. ) и электромагнитные поля различных частот (см. , ) , в том числеСВЧ ( ) .Э. проводят в виде местных и общих воздействий с наложением электродов на тело пациента (при процедурах с применением электрического тока) или без электродов (при использовании электромагнитных полей). Разнообразие факторов Э. и возможность менять их параметры позволяют индивидуализировать лечебные процедуры. Особенно рационально использование Э. в импульсном режиме, т. к. регулируемые частота и длительность импульсов обеспечивают нормализацию многих нарушенных физиологических процессов. В частности, импульсные токи низкой частоты могут имитировать эффекты нервных импульсов и оказывать на ткани трофическое влияние, нормализуя нарушенную нейроэндокринную регуляцию и избирательно стимулируя деятельность определённых органов и систем. При всех методах Э. проявляются общие, т. н. неспецифические, реакции - усиление кровообращения, обмена веществ, трофики тканей, компенсаторно-защитных свойств организма. Наряду с этим в ответ на действие каждого фактора возникают специфические реакции, проявления которых зависят от его физических свойств, методики применения и особенностей организма. Благодаря успехам в изучении лечебного действия физических факторов и достижениям электротехники и электромедицинского приборостроения Э. занимает значительное место в терапии многих заболеваний и реабилитации больных. Лит.:Аникин М. М., Варшавер Г. С., Основы физиотерапии, 2 изд., М., 1950; Ливенцев Н. М., Ливенсон А. Р., Электромедицинская аппаратура, 4 изд., М., 1974; Справочник по физиотерапии, под ред. А. Н. Обросова, М., 1976; Dumoulin J., Bisschop G. de, Electrotherapie, 2 ed., P., 1971; Edel H., Fibel der Elektrodiagnostik und Elektrptherapie, 3 Aufl., Dresden, 1975. В. М. Стругацкий. Электролиз Электро'лиз(от и греч. lysis - разложение, растворение, распад), совокупность процессов электрохимического на погруженных в электродах при прохождении через него электрического тока. Э. лежит в основе электрохимического метода лабораторного и промышленного получения различных веществ - как простых (Э. в узком смысле слова), так и сложных ( ) . Изучение и применение Э. началось в конце 18 - начале 19 вв., в период становления .Для разработки теоретических основ Э. большое значение имело установление М. в 1833-34 точных соотношений между количеством электричества, прошедшего при Э., и количеством вещества, выделившегося на электродах (см. ) .Промышленное применение Э. стало возможным после появления в 70-х гг. 19 в. мощных генераторов постоянного тока. Особенность Э. - пространственное разделение процессов окисления и восстановления: электрохимическое окисление происходит на аноде, восстановление - на катоде. Э. осуществляется в специальных аппаратах - . Э. происходит за счёт подводимой энергии постоянного тока и энергии, выделяющейся при химических превращениях на электродах. Энергия при Э. расходуется на повышение системы в процессе образования целевых продуктов и частично рассеивается в виде теплоты при преодолении сопротивлений в электролизёре и в других участках электрической цепи. На катоде в результате Э. происходит восстановление ионов или молекул электролита с образованием новых продуктов. Катионы принимают электроны и превращаются в ионы более низкой степени окисления или в атомы, например при восстановлении ионов железа (F 3+ e -® Fe 2+), электроосаждении меди (Cu 2++ 2 e- ® Cu). Нейтральные молекулы могут участвовать в превращениях на катоде непосредственно или реагировать с промежуточными продуктами катодного процесса. На аноде в результате Э. происходит окисление ионов или молекул, находящихся в электролите или принадлежащих материалу анода (анод растворяется или окисляется), например: выделение кислорода (4OH -® 4 e -+ 2H 2O + O 2) и хлора (2C1 -®2 e -+ Cl 2), образование хромата (Cr 3++ 3OH -+ H 2O ® CrO 4 2-+ 5H ++ 3 e -), растворение меди (Cu ® Cu 2++ 2 e- ), оксидирование алюминия (2Al + 3H 2O ® Al 2O 3+6Н ++ 6 e -). Электрохимическая реакция получения того или иного вещества (в атомарном, молекулярном или ионном состоянии) связана с переносом от электрода в электролит (или обратно) одного или нескольких зарядов в соответствии с уравнением химической реакции. В последнем случае такой процесс осуществляется, как правило, в виде последовательности элементарных одноэлектронных реакций, то есть постадийно, с образованием промежуточных ионов или радикальных частиц на электроде, часто остающихся на нём в адсорбированном состоянии. Скорости электродных реакций зависят от состава и концентрации электролита, от материала электрода, электродного потенциала, температуры и ряда других факторов. Скорость каждой электродной реакции определяется скоростью переноса электрических зарядов через единицу поверхности электрода в единицу времени; мерой скорости, следовательно, служит плотность тока. Количество образующихся при Э. продуктов определяется законами Фарадея. Если на каждом из электродов одновременно образуется ряд продуктов в результате нескольких электрохимических реакций, доля тока (в %), идущая на образование продукта одной из них, называется выходом данного продукта по току. Преимущества Э. перед химическим методами получения целевых продуктов заключаются в возможности сравнительно просто (регулируя ток) управлять скоростью и селективной направленностью реакций. Условия Э. легко контролировать, благодаря чему можно осуществлять процессы как в самых «мягких», так и в наиболее «жёстких» условиях окисления или восстановления, получать сильнейшие окислители и восстановители, используемые в науке и технике. Э. - основной метод промышленного производства алюминия, хлора и едкого натра, важнейший способ получения фтора, щелочных и щелочноземельных металлов, эффективный метод рафинирования металлов. Путём Э. воды производят водород и кислород. Электрохимический метод используется для синтеза органических соединений различных классов и многих окислителей (персульфатов, перманганатов, перхлоратов, перфторорганических соединений и др.). Применение Э. для обработки поверхностей включает как катодные процессы (в машиностроении, приборостроении, авиационной, электротехнической, электронной промышленности), так и анодные процессы полировки, травления, размерной ,оксидирования ( ) металлических изделий (см. также ) .Путём Э. в контролируемых условиях осуществляют защиту от коррозии металлических сооружений и конструкций (анодная и катодная защита). Лит.см. при ст. . Э. В. Касаткин. Электролизёры Электролизёры,аппараты для ,состоящие из одной или многих .Э. представляет собой сосуд (или систему сосудов), наполненный с размещенными в нём электродами - и ,соединёнными соответственно с отрицательным и положительным полюсами источника постоянного тока. В промышленности и лабораторной практике применяют Э. различных типов и конструкций (например, открытые и герметически закрытые, для периодической и непрерывной работы, с неподвижными и движущимися электродами, с различными системами разделения продуктов электролиза). В зависимости от назначения Э. рассчитываются для работы при различных температурах - от минусовых (при электрохимическом синтезе малостойких кислородных соединений) до высоких плюсовых (при электролизе расплавленных электролитов в производстве алюминия, кальция и др. металлов). Соответственно Э .снабжают устройствами для нагрева или охлаждения электролита пли электродов. Применяют Э. с диафрагмой - пористой перегородкой или мембраной, отделяющей катодное пространство от анодного, проницаемой для ионов, но затрудняющей механическое смешение и диффузию. Для изготовления диафрагм используются асбест, полимерные материалы и керамика, находят применения Э. с ионообменными мембранами. По способу включения в электрическую цепь Э. разделяются на моно- и биполярные. Монополярный Э. состоит из одной электролитической ячейки с электродами одной полярности, каждый из которых может состоять из нескольких элементов, включенных параллельно в цепь тока. Биполярный Э. имеет большое число ячеек (до 100-160), включенных последовательно в цепь тока, причём каждый электрод, за исключением двух крайних, работает одной стороной как катод, а другой как анод. Для изготовления анодов применяют графит, углеграфитовые материалы, платину, окислы некоторых металлов, свинец и его сплавы; используются малоизнашивающиеся титановые аноды с активным покрытием из смеси окислов рутения и титана, а также платины и её сплавов. Для катодов в большинстве Э. используется сталь. Применяются также Э. с жидкими электродами (например, в одном из методов производства хлора и гидроокиси натрия в качестве катода используют ртуть). Некоторые Э. работают под давлением, например разложение воды ведётся под давлением до 4 Мн/ м 2(40 кгс/ см 2) ;разрабатываются Э. для работы под более высоким давлением. Материалы для изготовления Э. выбираются с учётом агрессивности электролита и продуктов электролиза, температуры и других условий. Широко применяется сталь, в том числе с различными защитными покрытиями, пластические массы, стекло и стеклопластики, керамика. Современные крупные Э. имеют высокую нагрузку: монополярные до 400-500 ка,биполярные - эквивалентную 1600 ка. Л. М. Якименко. Электролитическая диссоциация Электролити'ческая диссоциа'ция,распад вещества на ионы при растворении. Э. д. происходит вследствие взаимодействия растворённого вещества с растворителем; по данным спектроскопических методов, это взаимодействие носит в значительной мере химический характер (см. ) .Наряду с сольватирующей способностью молекул растворителя определённую роль в Э. д. играет также макроскопическое свойство растворителя - его диэлектрическая проницаемость. Классическая теория Э. д. была создана С. и В. в 80-х гг. 19 в. Она основана на предположении о неполной диссоциации растворённого вещества, характеризуемой степенью диссоциации а, т. е. долей распавшихся молекул электролита. Динамическое равновесие между недиссоциированными молекулами и ионами описывается .Например, Э. д. бинарного электролита КА выражается уравнением типа КА Ы К ++ А -. Константа диссоциации К допределяется активностями катионов а К +,анионов а А- и недиссоциированных молекул а КАследующим образом:
Значение К дзависит от природы растворённого вещества и растворителя, а также от температуры и может быть определено несколькими экспериментальными методами. Степень диссоциации ее может быть рассчитана при любой концентрации a электролита с помощью соотношения:
где f ± -средний коэффициент активности электролита (см. также ) . Классическая теория Э. д. применима лишь к разбавленным растворам слабых электролитов. Сильные электролиты в разбавленных растворах диссоциированы практически полностью, поэтому представления о равновесии между ионами и недиссоциированными молекулами лишено смысла. Согласно представлениям, выдвинутым в 20-30-х гг. 20 в. В. К. Семенченко (СССР), Н. Бьеррумом (Дания), Р. М. Фуоссом (США) и др., в растворах сильных электролитов при средних и высоких концентрациях образуются ионные пары и более сложные агрегаты. Современные спектроскопические данные показывают, что ионная пара состоит из двух ионов противоположного знака, находящихся в контакте («контактная ионная пара») или разделённых одной или несколькими молекулами растворителя («разделённая ионная пара»). 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41 |
|||||||
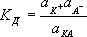 (1)
(1)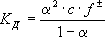 (2)
(2)