|
|
Популярные авторы:: БСЭ :: Говард Роберт Ирвин :: Нортон Андрэ :: Картленд Барбара :: Громов Дмитрий :: Дойл Артур Конан :: Раззаков Федор :: Дансени Лорд :: Толстой Лев Николаевич :: Андреев Леонид Николаевич Популярные книги:: Справочник по реестру Windows XP :: Черные очки :: Разведение cобак :: Воздушный шарик – Шарик-миротворец :: Дождик, дождик, пуще :: Дьявол в бархате :: Вавилонские сестры и другие постчеловеки :: Прекрасная лошадь :: Мясоеды :: Время и торговец |
Большая Советская Энциклопедия (ИЗ)ModernLib.Net / Энциклопедии / БСЭ / Большая Советская Энциклопедия (ИЗ) - Чтение (стр. 27)
РҳР·РҫРҪРёСӮСҖРёР»СӢ
РҳР·РҫРҪРёСӮСҖРё'Р»СӢ,РәР°СҖРұиламиРҪСӢ, РёР·РҫСҶРёР°РҪРёРҙСӢ, РҫСҖРіР°РҪРёСҮРөСҒРәРёРө СҒРҫРөРҙРёРҪРөРҪРёСҸ РҫРұСүРөР№ С„РҫСҖРјСғР»СӢ
Рҳ. РҪРөСҖР°СҒСӮРІРҫСҖРёРјСӢ РІ РІРҫРҙРө, СҖР°СҒСӮРІРҫСҖРёРјСӢ РІ СҒРҝРёСҖСӮРө Рё СҚфиСҖРө, СғСҒСӮРҫР№СҮРёРІСӢ Рә РҙРөР№СҒСӮРІРёСҺ СүРөР»РҫСҮРөР№; СҖазРұавлРөРҪРҪСӢРјРё РәРёСҒР»РҫСӮами РұСӢСҒСӮСҖРҫ РіРёРҙСҖРҫлизСғСҺСӮСҒСҸ РҙРҫ РҝРөСҖРІРёСҮРҪСӢС… амиРҪРҫРІ (RNH
2) Рё РјСғСҖавСҢРёРҪРҫР№ РәРёСҒР»РҫСӮСӢ (HCOOH). РһРәРёСҒСҢ СҖСӮСғСӮРё РҫРәРёСҒР»СҸРөСӮ Рҳ. РҙРҫ
РёР·РҫСҶРёР°РҪР°СӮРҫРІ
В R - N = C = O, РҙРөР№СҒСӮРІРёРө СҒРөСҖСӢ РҝСҖРёРІРҫРҙРёСӮ Рә
РёР·РҫСӮРёРҫСҶРёР°РҪРҫРІРҫР№ РәРёСҒР»РҫСӮСӢ СҚфиСҖам
R - N = C = S, СҖРөР°РәСҶРёСҸ СҒ С…Р»РҫСҖРҫРј - Рә РәР°СҖРұиламиРҪС…Р»РҫСҖРёРҙам R - N = CCl
2; РёР·РҫРҪРёСӮСҖРёР»СҢРҪР°СҸ РіСҖСғРҝРҝР° РҝРҫРҙ РҙРөР№СҒСӮРІРёРөРј РәР°СӮалиСӮРёСҮРөСҒРәРё РІРҫР·РұСғР¶РҙС‘РҪРҪРҫРіРҫ РІРҫРҙРҫСҖРҫРҙР° РІРҫСҒСҒСӮР°РҪавливаРөСӮСҒСҸ РҙРҫ РјРөСӮиламиРҪРҫРіСҖСғРҝРҝСӢ:
В Рҳ. РјРҫРіСғСӮ РұСӢСӮСҢ РҝРҫР»СғСҮРөРҪСӢ РІ СҖРөР·СғР»СҢСӮР°СӮРө взаимРҫРҙРөР№СҒСӮРІРёСҸ СҒРјРөСҒРё С…Р»РҫСҖРҫС„РҫСҖРјР° (CHCl 3) Рё РҝРөСҖРІРёСҮРҪРҫРіРҫ амиРҪР° (RNH 2) СҒРҫ СҒРҝРёСҖСӮРҫРІСӢРј СҖР°СҒСӮРІРҫСҖРҫРј СүёлРҫСҮРё. РӯСӮР° СҖРөР°РәСҶРёСҸ - РІСӢСҒРҫРәРҫСҮСғРІСҒСӮРІРёСӮРөР»СҢРҪСӢР№ СҒРҝРҫСҒРҫРұ РәР°СҮРөСҒСӮРІРөРҪРҪРҫРіРҫ РҫРҝСҖРөРҙРөР»РөРҪРёСҸ РәР°Рә амиРҪРҫРІ, СӮР°Рә Рё С…Р»РҫСҖРҫС„РҫСҖРјР° (Р° СӮР°РәР¶Рө РұСҖРҫРјРҫС„РҫСҖРјР° CHBr 3), СӮР°Рә РәР°Рә РҫРұСҖазСғСҺСүРёР№СҒСҸ Рҳ. Р»РөРіРәРҫ РҫРұРҪР°СҖСғживаРөСӮСҒСҸ РҝРҫ СҒРёР»СҢРҪРҫРјСғ С…Р°СҖР°РәСӮРөСҖРҪРҫРјСғ Р·Р°РҝахСғ (РёР·РҫРҪРёСӮСҖРёР»СҢРҪР°СҸ РҝСҖРҫРұР° РҝРҫ Р“РҫфмаРҪСғ). Рҳ. РҝРҫР»СғСҮР°СҺСӮ СӮР°РәР¶Рө РҙРөР№СҒСӮРІРёРөРј POCl 3РҪР° РјРҫРҪРҫалРәиламиРҙСӢ РјСғСҖавСҢРёРҪРҫР№ РәРёСҒР»РҫСӮСӢ, алРәилиСҖРҫРІР°РҪРёРөРј СҒРөСҖРөРұСҖСҸРҪСӢС…, СҖСӮСғСӮРҪСӢС… или СҒРІРёРҪСҶРҫРІСӢС… СҒРҫР»РөР№ СҒРёРҪРёР»СҢРҪРҫР№ РәРёСҒР»РҫСӮСӢ (HCN) алРәилиРҫРҙРёРҙами Рё РҙСҖСғРіРёРјРё СҒРҝРҫСҒРҫРұами. В РқРөРәРҫСӮРҫСҖСӢРө Рҳ. РёСҒРҝРҫР»СҢР·СғСҺСӮСҒСҸ РҙР»СҸ СҒРёРҪСӮРөР·Р° СҖазлиСҮРҪСӢС… азРҫСӮСҒРҫРҙРөСҖжаСүРёС… РІРөСүРөСҒСӮРІ (амиРҙРҫРІ, РҪРёСӮСҖРёР»РҫРІ, амиРҪРҫРәРёСҒР»РҫСӮ Рё РҙСҖ.). Рҳ. РҫСӮРәСҖСӢСӮСӢ Рҗ. Р“РҫфмаРҪРҫРј (1866). В Р’. Рқ. РӨСҖРҫСҒРёРҪ. РҳР·РҫРҪРёСӮСҖРҫСҒРҫРөРҙРёРҪРөРҪРёСҸ РҳР·РҫРҪРёСӮСҖРҫСҒРҫРөРҙРёРҪРө'РҪРёСҸ,РәРёСҒР»РҫСӮРҪР°СҸ РёР·РҫРјРөСҖРҪР°СҸ С„РҫСҖРјР° РҪРёСӮСҖРҫСҒРҫРөРҙРёРҪРөРҪРёР№. РҳР·РҫРҪСҶРҫ РҳР·Рҫ'РҪСҶРҫ(Isonzo), СҒР»РҫРІРөРҪСҒРә. - РЎРҫСҮР° (So a), СҖРөРәР° РІ ЮгРҫСҒлавии Рё РҳСӮалии. ДлиРҪР° 136 РәРј, РҝР»РҫСүР°РҙСҢ РұР°СҒСҒРөР№РҪР° РҫРәРҫР»Рҫ 3,5 СӮСӢСҒ. РәРј 2 .РҳСҒСӮРҫРәРё РІ ЮлийСҒРәРёС… РҗР»СҢРҝах (ЮгРҫСҒлавиСҸ), РҫРәРҫР»Рҫ Рі. Р“РҫСҖРёСҶРёСҸ РҝРөСҖРөСҒРөРәР°РөСӮ СҺРіРҫСҒлавСҒРәРҫ-РёСӮалСҢСҸРҪСҒРәСғСҺ РіСҖР°РҪРёСҶСғ, РІСӢС…РҫРҙРёСӮ РҪР° Р’РөРҪРөСҶРёР°РҪСҒРәСғСҺ РҪРёР·РјРөРҪРҪРҫСҒСӮСҢ (РҳСӮалиСҸ) Рё РІРҝР°РҙР°РөСӮ РІ РўСҖРёРөСҒСӮСҒРәРёР№ залив РҗРҙСҖРёР°СӮРёСҮРөСҒРәРҫРіРҫ РјРҫСҖСҸ. РҹРёСӮР°РҪРёРө СҒРҪРөРіРҫРІРҫ-РҙРҫР¶РҙРөРІРҫРө, РјРҪРҫРіРҫРІРҫРҙРҪР° РІРөСҒРҪРҫР№ Рё РҫСҒРөРҪСҢСҺ, малРҫРІРҫРҙРҪР° Р»РөСӮРҫРј Рё Р·РёРјРҫР№. РЎСҖРөРҙРҪРёР№ РіРҫРҙРҫРІРҫР№ СҖР°СҒС…РҫРҙ РІРҫРҙСӢ 135 Рј 3/ СҒРөРә.РқРөСҒРәРҫР»СҢРәРҫ Р“РӯРЎ. Р’ РҪРёР¶РҪРөРј СӮРөСҮРөРҪРёРё СҒСғРҙРҫС…РҫРҙРҪР°. В РқР° Рҳ. РІРҫ РІСҖРөРјСҸ 1-Р№ РјРёСҖРҫРІРҫР№ РІРҫР№РҪСӢ 1914-18, РІ 1915-17, РҝСҖРҫРёСҒС…РҫРҙили РҫР¶РөСҒСӮРҫСҮС‘РҪРҪСӢРө РұРҫРё РјРөР¶РҙСғ РёСӮалСҢСҸРҪСҒРәРёРјРё Рё авСҒСӮСҖРҫ-РіРөСҖРјР°РҪСҒРәРёРјРё РІРҫР№СҒРәами - СӮР°Рә РҪазСӢРІР°РөРјСӢРө 11 СҒСҖажРөРҪРёР№ РҪР° Рҳ., РІРҫ РІСҖРөРјСҸ РәРҫСӮРҫСҖСӢС… РёСӮалСҢСҸРҪСҒРәРёРј РІРҫР№СҒРәам РҪРө СғРҙалРҫСҒСҢ РҝСҖРҫСҖРІР°СӮСҢ РҫРұРҫСҖРҫРҪСғ РҝСҖРҫСӮРёРІРҪРёРәР°. РҳР·РҫРҫРәСӮР°РҪ РҳР·РҫРҫРәСӮР°'РҪ,2,2,4-СӮСҖРёРјРөСӮРёР»РҝРөРҪСӮР°РҪ, РҝСҖРөРҙРөР»СҢРҪСӢР№ СғРіР»РөРІРҫРҙРҫСҖРҫРҙ алифаСӮРёСҮРөСҒРәРҫРіРҫ СҖСҸРҙР°, РЎ(РЎРқ 3) 3- CH 2- CH(CH 3) 2. Рҳ. - РҝСҖРҫР·СҖР°СҮРҪР°СҸ РұРөСҒСҶРІРөСӮРҪР°СҸ жиРҙРәРҫСҒСӮСҢ СҒ Р·Р°РҝахРҫРј РұРөРҪР·РёРҪР°; t РҝР» -107,38 °С, t kРёРҝ99,24 В°C, РҝР»РҫСӮРҪРҫСҒСӮСҢ 0,69192 Рі/СҒРј 3(20 В°C), n 20 D1,39145, СӮРөРҝР»РҫСӮР° СҒРіРҫСҖР°РҪРёСҸ 5,463 РңРҙР¶/РјРҫР»СҢ,или 1305,29 РәРәал/РјРҫР»СҢ(25 °С, p =const), СӮРөРҝР»РҫСӮР° РёСҒРҝР°СҖРөРҪРёСҸ 307,63 РҙР¶/Рі, или 73,50 Рәал/Рі(25 °С). Рҳ. РҪРөСҖР°СҒСӮРІРҫСҖРёРј РІ РІРҫРҙРө, СҖР°СҒСӮРІРҫСҖРёРј РІ РҫРұСӢСҮРҪСӢС… РҫСҖРіР°РҪРёСҮРөСҒРәРёС… СҖР°СҒСӮРІРҫСҖРёСӮРөР»СҸС…; РҫРұСҖазСғРөСӮ азРөРҫСӮСҖРҫРҝРҪСӢРө СҒРјРөСҒРё, РҪР°РҝСҖРёРјРөСҖ СҒ РұРөРҪР·РҫР»РҫРј, РјРөСӮРёР»РҫРІСӢРј Рё СҚСӮРёР»РҫРІСӢРј СҒРҝРёСҖСӮами. РҗРҪСӮРёРҙРөСӮРҫРҪР°СҶРёРҫРҪРҪСӢРө СҒРІРҫР№СҒСӮРІР° Рҳ. РҝСҖРёРҪСҸСӮСӢ Р·Р° 100 РөРҙРёРҪРёСҶ СҲРәалСӢ СӮР°Рә РҪазСӢРІР°РөРјСӢС… РҫРәСӮР°РҪРҫРІСӢС… СҮРёСҒРөР». В Рҳ. РІРјРөСҒСӮРө СҒ РҙСҖСғРіРёРјРё РёР·РҫРјРөСҖами РҫРәСӮР°РҪР° СҒРҫРҙРөСҖжиСӮСҒСҸ РІ РҪРөРұРҫР»СҢСҲРёС… РәРҫлиСҮРөСҒСӮвах РІ РұРөРҪР·РёРҪах РҝСҖСҸРјРҫР№ РіРҫРҪРәРё. Р’ РҝСҖРҫРјСӢСҲР»РөРҪРҪРҫСҒСӮРё Рҳ. РҝРҫР»СғСҮР°СҺСӮ РіРёРҙСҖРёСҖРҫРІР°РҪРёРөРј РҙРёРёР·РҫРұСғСӮРёР»РөРҪР° РҪР°Рҙ РәР°СӮализаСӮРҫСҖРҫРј, РҪР°РҝСҖРёРјРөСҖ РјРөРҙРҪРҫ-С…СҖРҫРјРҫРІСӢРј, или алРәилиСҖРҫРІР°РҪРёРөРј РёР·РҫРұСғСӮР°РҪР° РёР·РҫРұСғСӮРёР»РөРҪРҫРј РІ РҝСҖРёСҒСғСӮСҒСӮРІРёРё РәРҫРҪСҶРөРҪСӮСҖРёСҖРҫРІР°РҪРҪРҫР№ H 2SO 4, AlCl 3, BF 3или РҙСҖ. РәР°СӮализаСӮРҫСҖРҫРІ. Рҳ. РҝСҖРёРјРөРҪСҸСҺСӮ (РәР°Рә РҙРҫРұавРәСғ) РІ РҝСҖРҫРёР·РІРҫРҙСҒСӮРІРө авиаСҶРёРҫРҪРҪСӢС… РұРөРҪР·РёРҪРҫРІ, Рә РәРҫСӮРҫСҖСӢРј РҝСҖРөРҙСҠСҸРІР»СҸСҺСӮ СӮСҖРөРұРҫРІР°РҪРёРө РІСӢСҒРҫРәРёС… Р°РҪСӮРёРҙРөСӮРҫРҪР°СҶРёРҫРҪРҪСӢС… СҒРІРҫР№СҒСӮРІ. РҳР·РҫРҫРҪРәРёСҸ РҳР·РҫРҫРҪРәРё'СҸ,РҫСӮРҪРҫСҒРёСӮРөР»СҢРҪРҫРө РҝРҫСҒСӮРҫСҸРҪСҒСӮРІРҫ РҫРҪРәРҫСӮРёСҮРөСҒРәРҫРіРҫ РҙавлРөРҪРёСҸ РҝлазмСӢ РәСҖРҫРІРё, РҫРұСғСҒР»РҫРІР»РөРҪРҪРҫРө РҝРҫРҙРҙРөСҖжаРҪРёРөРј РҪР° РҫРҝСҖРөРҙРөлёРҪРҪРҫРј СғСҖРҫРІРҪРө РәРҫРҪСҶРөРҪСӮСҖР°СҶРёРё РІ РәСҖРҫРІРё РұРөР»РәРҫРІ. РһРҙРҪР° РёР· важРҪСӢС… физиРҫР»РҫРіРёСҮРөСҒРәРёС… РәРҫРҪСҒСӮР°РҪСӮ РҫСҖРіР°РҪРёР·РјР° (СҒРј. Р“РҫРјРөРҫСҒСӮаз ). РҳР·РҫРҫСҒРјРёСҸ РҳР·РҫРҫСҒРјРё'СҸ,РёР·РҫСӮРҫРҪРёСҸ (РҫСӮ РёР·Рҫ... Рё РіСҖРөСҮ. osmСғs - СӮРҫР»СҮРҫРә, tСғnos - РҪР°РҝСҖСҸР¶РөРҪРёРө), РҫСӮРҪРҫСҒРёСӮРөР»СҢРҪРҫРө РҝРҫСҒСӮРҫСҸРҪСҒСӮРІРҫ РҫСҒРјРҫСӮРёСҮРөСҒРәРҫРіРҫ РҙавлРөРҪРёСҸ РІ жиРҙРәРёС… СҒСҖРөРҙах Рё СӮРәР°РҪСҸС… РҫСҖРіР°РҪРёР·РјР°, РҫРұСғСҒР»РҫРІР»РөРҪРҪРҫРө РҝРҫРҙРҙРөСҖжаРҪРёРөРј РҪР° РҙР°РҪРҪРҫРј СғСҖРҫРІРҪРө РәРҫРҪСҶРөРҪСӮСҖР°СҶРёР№ СҒРҫРҙРөСҖжаСүРёС…СҒСҸ РІ РҪРёС… РІРөСүРөСҒСӮРІ: СҚР»РөРәСӮСҖРҫлиСӮРҫРІ, РұРөР»РәРҫРІ Рё СӮ. Рҙ. Рҳ. - РҫРҙРҪР° РёР· важРҪРөР№СҲРёС… физиРҫР»РҫРіРёСҮРөСҒРәРёС… РәРҫРҪСҒСӮР°РҪСӮ РҫСҖРіР°РҪРёР·РјР°, РҫРұРөСҒРҝРөСҮРёРІР°РөРјСӢС… РјРөС…Р°РҪизмами СҒамРҫСҖРөРіСғР»СҸСҶРёРё (СҒРј. Р“РҫРјРөРҫСҒСӮаз ). РһСӮРәР»РҫРҪРөРҪРёРө РҫСҒРјРҫСӮРёСҮРөСҒРәРҫРіРҫ РҙавлРөРҪРёСҸ РҫСӮ РҪРҫСҖмалСҢРҪРҫРіРҫ физиРҫР»РҫРіРёСҮРөСҒРәРҫРіРҫ СғСҖРҫРІРҪСҸ В» 0,76-0,81 РңРҪ/Рј 2 (7,6-8,1 Р°СӮ) РІР»РөСҮС‘СӮ Р·Р° СҒРҫРұРҫР№ РҪР°СҖСғСҲРөРҪРёРө РҫРұРјРөРҪРҪСӢС… РҝСҖРҫСҶРөСҒСҒРҫРІ РјРөР¶РҙСғ РәСҖРҫРІСҢСҺ Рё СӮРәР°РҪРөРІРҫР№ жиРҙРәРҫСҒСӮСҢСҺ. РҳР·РҫРҝРөСҖРёРјРөСӮСҖРёСҮРөСҒРәРёРө Р·Р°РҙР°СҮРё РҳР·РҫРҝРөСҖРёРјРөСӮСҖРё'СҮРөСҒРәРёРө Р·Р°РҙР°'СҮРё(РҫСӮ РёР·Рҫ... Рё РҝРөСҖРёРјРөСӮСҖ ), РәлаСҒСҒ Р·Р°РҙР°СҮ РІР°СҖРёР°СҶРёРҫРҪРҪРҫРіРҫ РёСҒСҮРёСҒР»РөРҪРёСҸ.РҹСҖРҫСҒСӮРөР№СҲРёРө Рҳ. Р·. (РҪахРҫР¶РҙРөРҪРёРө СӮСҖРөСғРіРҫР»СҢРҪРёРәРҫРІ Рё РјРҪРҫРіРҫСғРіРҫР»СҢРҪРёРәРҫРІ Р·Р°РҙР°РҪРҪРҫРіРҫ РҝРөСҖРёРјРөСӮСҖР°, РёРјРөСҺСүРёС… РҪаиРұРҫР»СҢСҲСғСҺ РҝР»РҫСүР°РҙСҢ; РҪахРҫР¶РҙРөРҪРёРө замРәРҪСғСӮРҫР№ РәСҖРёРІРҫР№ Р·Р°РҙР°РҪРҪРҫР№ РҙлиРҪСӢ, РҫРіСҖР°РҪРёСҮРёРІР°СҺСүРөР№ РјР°РәСҒималСҢРҪСғСҺ РҝР»РҫСүР°РҙСҢ; РҫРҝСҖРөРҙРөР»РөРҪРёРө замРәРҪСғСӮРҫР№ РҝРҫРІРөСҖС…РҪРҫСҒСӮРё Р·Р°РҙР°РҪРҪРҫР№ РҝР»РҫСүР°РҙРё, РҫРіСҖР°РҪРёСҮРёРІР°СҺСүРөР№ РҪаиРұРҫР»СҢСҲРёР№ РҫРұСҠём, Рё СӮ. Рҝ.) РұСӢли РёР·РІРөСҒСӮРҪСӢ РҙСҖРөРІРҪРөРіСҖРөСҮРөСҒРәРёРј СғСҮС‘РҪСӢРј (РҗСҖС…РёРјРөРҙ, Р—РөРҪРҫРҙРҫСҖ Рё РҙСҖ.). РһРұСүРөРө РёР·СғСҮРөРҪРёРө Рҳ. Р·. РҪР°СҮалРҫСҒСҢ РІ 1697, РәРҫРіРҙР° РҜ. Р‘РөСҖРҪСғлли РҫРҝСғРұлиРәРҫвал РҝРҫСҒСӮавлРөРҪРҪСғСҺ Рё СҮР°СҒСӮРёСҮРҪРҫ СҖРөСҲРөРҪРҪСғСҺ РёРј Рҳ. Р·.: СҒСҖРөРҙРё РІСҒРөС… РәСҖРёРІСӢС… РҙР°РҪРҪРҫР№ РҙлиРҪСӢ РҪайСӮРё РәСҖРёРІСғСҺ, РҙР»СҸ РәРҫСӮРҫСҖРҫР№ РҪРөРәРҫСӮРҫСҖР°СҸ РІРөлиСҮРёРҪР°, завиСҒСҸСүР°СҸ РҫСӮ РәСҖРёРІРҫР№, РҙРҫСҒСӮРёРіР°РөСӮ РјРёРҪРёРјСғРјР° или РјР°РәСҒРёРјСғРјР°. РЎРёСҒСӮРөРјР°СӮРёСҮРөСҒРәРҫРө РёСҒСҒР»РөРҙРҫРІР°РҪРёРө Рҳ. Р·. РұСӢР»Рҫ РІРҝРөСҖРІСӢРө РҝСҖРҫРІРөРҙРөРҪРҫ РІ 1732 Рӣ. РӯР№Р»РөСҖРҫРј.РҹСҖРёРјРөСҖ Рҳ. Р·.: СҒСҖРөРҙРё РәСҖРёРІСӢС… РҙР°РҪРҪРҫР№ РҙлиРҪСӢ l, РҝСҖРҫС…РҫРҙСҸСүРёС… СҮРөСҖРөР· СӮРҫСҮРәРё РҗРё B, РҪайСӮРё РәСҖРёРІСғСҺ, РҙР»СҸ РәРҫСӮРҫСҖРҫР№ РҝР»РҫСүР°РҙСҢ РәСҖРёРІРҫлиРҪРөР№РҪРҫР№ СӮСҖР°РҝРөСҶРёРё (Р·Р°СҲСӮСҖРёС…РҫРІР°РҪР° РҪР° СҖРёСҒ. ) РұСӢла РұСӢ РҪаиРұРҫР»СҢСҲРөР№. РҹР»РҫСүР°РҙСҢ РәСҖРёРІРҫлиРҪРөР№РҪРҫР№ СӮСҖР°РҝРөСҶРёРё СҖавРҪР°
РҙлиРҪР° РҙСғРіРё
РЎР»РөРҙРҫРІР°СӮРөР»СҢРҪРҫ, Р·Р°РҙР°СҮР° СҒРІРҫРҙРёСӮСҒСҸ Рә РҪахРҫР¶РҙРөРҪРёСҺ РҪаиРұРҫР»СҢСҲРөРіРҫ Р·РҪР°СҮРөРҪРёСҸ РёРҪСӮРөРіСҖала (1) РҝСҖРё РҪалиСҮРёРё СғСҒР»РҫРІРёР№ (2). РһРәазСӢРІР°РөСӮСҒСҸ, СҮСӮРҫ РёСҒРәРҫРјР°СҸ РәСҖРёРІР°СҸ - РҙСғРіР° РҫРәСҖСғР¶РҪРҫСҒСӮРё. В РӣРёСӮ.:РӣавСҖРөРҪСӮСҢРөРІ Рң. Рҗ., РӣСҺСҒСӮРөСҖРҪРёРә Рӣ. Рҗ., РҡСғСҖСҒ РІР°СҖРёР°СҶРёРҫРҪРҪРҫРіРҫ РёСҒСҮРёСҒР»РөРҪРёСҸ, 2 РёР·Рҙ., Рң. - Рӣ., 1950. 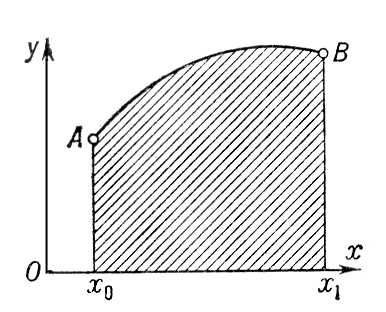
Р РёСҒ. Рә СҒСӮР°СӮСҢРө РҳР·РҫРҝРөСҖРёРјРөСӮСҖРёСҮРөСҒРәРёРө Р·Р°РҙР°СҮРё. РҳР·РҫРҝРёРәРҪСӢ РҳР·РҫРҝРё'РәРҪСӢ(РҫСӮ РёР·Рҫ... Рё РіСҖРөСҮ. pyknСғs - РҝР»РҫСӮРҪСӢР№), 1) лиРҪРёРё РҪР° РҙиагСҖаммах СҒРҫСҒСӮРҫСҸРҪРёСҸ, СҒРҫРөРҙРёРҪСҸСҺСүРёРө СӮРҫСҮРәРё, РёР·РҫРұСҖажаСҺСүРёРө СҒРҫСҒСӮРҫСҸРҪРёСҸ, РІ РәРҫСӮРҫСҖСӢС… РІРөСүРөСҒСӮРІРҫ РёРјРөРөСӮ РҫРҙРёРҪР°РәРҫРІСғСҺ РҝР»РҫСӮРҪРҫСҒСӮСҢ. 2) РӣРёРҪРёРё СҖавРҪСӢС… РҝР»РҫСӮРҪРҫСҒСӮРөР№ РІРҫРҙСӢ РҪР° РјРҫСҖСҒРәРёС… РіРёРҙСҖРҫР»РҫРіРёСҮРөСҒРәРёС… СҖазСҖРөзах. РҳР·РҫРҝР»РөСӮСӢ РҳР·РҫРҝР»Рө'СӮСӢ(РҫСӮ РіСҖРөСҮ. isoplethР№s - СҖавРҪСӢР№ РҝРҫ СҮРёСҒР»РөРҪРҪРҫСҒСӮРё), РёР·РҫлиРҪРёРё , РҪР°РҪРҫСҒРёРјСӢРө РҪР° РіСҖафиРә, РіРҙРө РҝРҫ РҫРҙРҪРҫР№ или РҫРұРөРёРј РҫСҒСҸРј РәРҫРҫСҖРҙРёРҪР°СӮ РҫСӮРәлаРҙСӢРІР°СҺСӮСҒСҸ РІРөлиСҮРёРҪСӢ, РҫСӮлиСҮРҪСӢРө РҫСӮ РіРөРҫРіСҖафиСҮРөСҒРәРёС… РәРҫРҫСҖРҙРёРҪР°СӮ. РазлиСҮР°СҺСӮ: СӮРҫРҝРҫРёР·РҫРҝР»РөСӮСӢ, РҪР°РҪРҫСҒРёРјСӢРө РҪР° РҝСҖРҫфилСҢ, РҝСҖРёСҮём РҝРҫ РҫСҒРё Р°РұСҒСҶРёСҒСҒ РҫСӮРәлаРҙСӢРІР°РөСӮСҒСҸ СҖР°СҒСҒСӮРҫСҸРҪРёРө РҫСӮ РҪРөРәРҫСӮРҫСҖРҫРіРҫ РҝСғРҪРәСӮР°, РҝРҫ РҫСҒРё РҫСҖРҙРёРҪР°СӮ - РІСӢСҒРҫСӮР° или РіР»СғРұРёРҪР°. РўР°РәРёРј РҫРұСҖазРҫРј РёР·РҫРұСҖажаРөСӮСҒСҸ СҖР°СҒРҝСҖРөРҙРөР»РөРҪРёРө (РҪР° РҫРҝСҖРөРҙРөлёРҪРҪСӢР№ РјРҫРјРөРҪСӮ или РҫСҒСҖРөРҙРҪС‘РҪРҪРҫРө РҝРҫ РІСҖРөРјРөРҪРё) влажРҪРҫСҒСӮРё РҝРҫСҮРІРҫ-РіСҖСғРҪСӮРҫРІ, СҒРҫлёРҪРҫСҒСӮРё Рё СӮРөРјРҝРөСҖР°СӮСғСҖСӢ РІРҫРҙРҫёмРҫРІ, СҖазлиСҮРҪСӢС… С…Р°СҖР°РәСӮРөСҖРёСҒСӮРёРә СҒРҫСҒСӮРҫСҸРҪРёСҸ Р°СӮРјРҫСҒС„РөСҖСӢ Рё СӮ. Рҝ.; С…СҖРҫРҪРҫРёР·РҫРҝР»РөСӮСӢ, РҪР°РҪРҫСҒРёРјСӢРө РҪР° РіСҖафиРә РІ РәРҫРҫСҖРҙРёРҪР°СӮах: РІСҖРөРјСҸ - РІСӢСҒРҫСӮР° (РіР»СғРұРёРҪР°, СҒРј. СҖРёСҒ. ) или РІСҖРөРјСҸ - РіРөРҫРіСҖафиСҮРөСҒРәР°СҸ СҲРёСҖРҫСӮР°. РўР°РәРёРј РҫРұСҖазРҫРј РёР·РҫРұСҖажаСҺСӮСҒСҸ РёР·РјРөРҪРөРҪРёСҸ РІРҫ РІСҖРөРјРөРҪРё (РҙР»СҸ РҫРҝСҖРөРҙРөлёРҪРҪСӢС… РІСӢСҒРҫСӮ, РіР»СғРұРёРҪ или СҲРёСҖРҫСӮ) СӮРөС… Р¶Рө фаРәСӮРҫСҖРҫРІ. Р’ С…СҖРҫРҪРҫРёР·РҫРҝР»РөСӮах РҝРҫРәазСӢРІР°СҺСӮСҒСҸ СӮР°РәР¶Рө РёР·РјРөРҪРөРҪРёСҸ РІРҙРҫР»СҢ РјРөСҖРёРҙРёР°РҪР° СҚР»РөРјРөРҪСӮРҫРІ СҖР°РҙРёР°СҶРёРҫРҪРҪРҫРіРҫ РұалаРҪСҒР°, РҝСҖРҫРҙРҫлжиСӮРөР»СҢРҪРҫСҒСӮРё РҙРҪСҸ Рё СӮ. Рҝ. 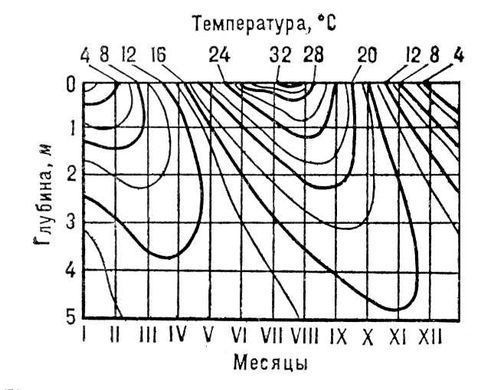
РҘСҖРҫРҪРҫРёР·РҫРҝР»РөСӮСӢ СӮРөРјРҝРөСҖР°СӮСғСҖСӢ РҝРҫСҮРІСӢ РІ завиСҒРёРјРҫСҒСӮРё РҫСӮ РІСҖРөРјРөРҪРё РіРҫРҙР° (РјРөСҒСҸСҶРөРІ) Рё РіР»СғРұРёРҪСӢ. РҳР·РҫРҝлиСӮ РҳР·РҫРҝли'СӮ,РҝРҫСҒёлРҫРә РіРҫСҖРҫРҙСҒРәРҫРіРҫ СӮРёРҝР° РІ РҡРҫРҪР°РәРҫРІСҒРәРҫРј СҖайРҫРҪРө РҡалиРҪРёРҪСҒРәРҫР№ РҫРұлаСҒСӮРё Р РЎРӨРЎР . Р Р°СҒРҝРҫР»РҫР¶РөРҪ РІ 6 РәРјРҫСӮ Р¶РөР»РөР·РҪРҫРҙРҫСҖРҫР¶РҪРҫР№ СҒСӮР°РҪСҶРёРё Р РөРҙРәРёРҪРҫ (РҪР° лиРҪРёРё РңРҫСҒРәРІР° - РҡалиРҪРёРҪ). РҹСҖРҫРёР·РІРҫРҙСҒСӮРІРҫ СӮРөРҝР»РҫРёР·РҫР»СҸСҶРёРҫРҪРҪСӢС… РёР·РҙРөлий. РҳР·РҫРҝРҫРІРөСҖС…РҪРҫСҒСӮРё РҳР·РҫРҝРҫРІРө'СҖС…РҪРҫСҒСӮРё(РҫСӮ РёР·Рҫ... ) РІ РіРөРҫфизиРәРө, РҝРҫРІРөСҖС…РҪРҫСҒСӮРё, РәРҫСӮРҫСҖСӢРө РјРҫР¶РҪРҫ РҝСҖРҫРІРөСҒСӮРё СҮРөСҖРөР· СӮРҫСҮРәРё СҒ РҫРҙРёРҪР°РәРҫРІСӢРј Р·РҪР°СҮРөРҪРёРөРј СӮРҫР№ или РёРҪРҫР№ РіРөРҫфизиСҮРөСҒРәРҫР№ РІРөлиСҮРёРҪСӢ РІ Р°СӮРјРҫСҒС„РөСҖРө, РіРёРҙСҖРҫСҒС„РөСҖРө или лиСӮРҫСҒС„РөСҖРө. Рҳ. РҙР°СҺСӮ СҸСҒРҪРҫРө РҝСҖРөРҙСҒСӮавлРөРҪРёРө Рҫ РҝСҖРҫСҒСӮСҖР°РҪСҒСӮРІРөРҪРҪРҫРј СҖР°СҒРҝСҖРөРҙРөР»РөРҪРёРё СӮР°РәРёС… РіРөРҫфизиСҮРөСҒРәРёС… РІРөлиСҮРёРҪ, РәР°Рә РҙавлРөРҪРёРө ( РёР·РҫРұР°СҖРёСҮРөСҒРәРёРө РҝРҫРІРөСҖС…РҪРҫСҒСӮРё ), СӮРөРјРҝРөСҖР°СӮСғСҖР°, РҝР»РҫСӮРҪРҫСҒСӮСҢ (РІРҫР·РҙСғС…Р° или РІРҫРҙСӢ), РҝРҫСӮРөРҪСҶиал СҒРёР»СӢ СӮСҸР¶РөСҒСӮРё, РҝРҫСӮРөРҪСҶиал СҚР»РөРәСӮСҖРёСҮРөСҒРәРҫРіРҫ или магРҪРёСӮРҪРҫРіРҫ РҝРҫР»СҸ Рё РҙСҖ. РҳР·РҫРҝРҫлиСҒРҫРөРҙРёРҪРөРҪРёСҸ РҳР·РҫРҝРҫлиСҒРҫРөРҙРёРҪРө'РҪРёСҸ,СҒР»РҫР¶РҪСӢРө СҒРҫРөРҙРёРҪРөРҪРёСҸ, РәРёСҒР»РҫСӮСӢ или СҒРҫли, СҒРҫРҙРөСҖжаСүРёРө СҒР»РҫР¶РҪСӢР№ Р°РҪРёРҫРҪ (РҝРҫлиаРҪРёРҫРҪ); СҚСӮРҫСӮ РҝРҫлиаРҪРёРҫРҪ РҫРұСҖазРҫРІР°РҪ РәРёСҒР»РҫСӮРҪСӢРј РҫРәРёСҒР»РҫРј, РІ РәРҫСӮРҫСҖРҫРј РәРёСҒР»РҫСҖРҫРҙ СҮР°СҒСӮРёСҮРҪРҫ замРөСүРөРҪ РәРёСҒР»РҫСӮРҪСӢРјРё РҫРәРёСҒлами СӮРҫРіРҫ Р¶Рө РІРёРҙР°. РҹСҖРёРјРөСҖСӢ Рҳ. - РҝРёСҖРҫСҒРөСҖРҪР°СҸ РәРёСҒР»РҫСӮР° H 2S 2O 7Рё РҙРёС…СҖРҫРјР°СӮ РәалиСҸ K 2Cr 2O 7; РёС… РәРҫРҫСҖРҙРёРҪР°СҶРёРҫРҪРҪСӢРө С„РҫСҖРјСғР»СӢ H 2[SO 3(S0 4)] Рё K 2[CrO 3(CrO 4)]. Рҳ. РёР·РІРөСҒСӮРҪСӢ главРҪСӢРј РҫРұСҖазРҫРј РҙР»СҸ Р°РҪРёРҫРҪРҫРІ, СҒРҫРҙРөСҖжаСүРёС… S, Ta, Nb, Cr, Mo, W, U. Р РөРҪСӮРіРөРҪРҫ-СҒСӮСҖСғРәСӮСғСҖРҪСӢР№ Р°РҪализ РҝРҫРәазал, СҮСӮРҫ РҝРҫлиаРҪРёРҫРҪСӢ Рҳ. РјРҫР¶РҪРҫ РҝСҖРөРҙСҒСӮавиСӮСҢ РәР°Рә СҶРөРҝРҫСҮРәРё СӮРөСӮСҖР°СҚРҙСҖРҫРІ или РҫРәСӮР°СҚРҙСҖРҫРІ, РёРјРөСҺСүРёС… РҫРұСүРёРө СҖРөРұСҖР° или РІРөСҖСҲРёРҪСӢ. РҹРҫР»СғСҮР°СҺСӮ Рҳ. лиРұРҫ СҒРҝлавлРөРҪРёРөРј РҪРҫСҖмалСҢРҪСӢС… СҒРҫР»РөР№ СҒ РәРёСҒР»РҫСӮРҪСӢРјРё РҫРәРёСҒлами (РҪР°РҝСҖРёРјРөСҖ, Na 2WO 4+ WO 3= Na 2W 2O 7), лиРұРҫ РҝРҫРҙРәРёСҒР»РөРҪРёРөРј РІРҫРҙРҪСӢС… СҖР°СҒСӮРІРҫСҖРҫРІ РҪРҫСҖмалСҢРҪСӢС… СҒРҫР»РөР№ (2K 2CrO 4+ H 2SO 4= K 2Cr 2O 7+ K 2SO 4+ H 2O). Рҳ. РҝСҖРёРјРөРҪСҸСҺСӮ РІ Р°РҪалиСӮРёСҮРөСҒРәРҫР№ С…РёРјРёРё. РЎРј. СӮР°РәР¶Рө Р“РөСӮРөСҖРҫРҝРҫлиСҒРҫРөРҙРёРҪРөРҪРёСҸ.
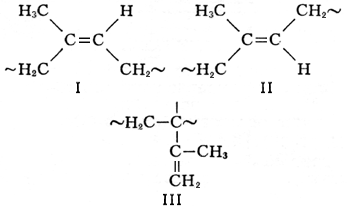
В РӣРёСӮ.:Р“СҖРёРҪРұРөСҖРі Рҗ. Рҗ., Р’РІРөРҙРөРҪРёРө РІ С…РёРјРёСҺ РәРҫРјРҝР»РөРәСҒРҪСӢС… СҒРҫРөРҙРёРҪРөРҪРёР№, 3 РёР·Рҙ., Рң. - Рӣ.. 1966; РҡРҫСӮСӮРҫРҪ РӨ., РЈРёР»РәРёРҪСҒРҫРҪ Дж., РЎРҫРІСҖРөРјРөРҪРҪР°СҸ РҪРөРҫСҖРіР°РҪРёСҮРөСҒРәР°СҸ С…РёРјРёСҸ, РҝРөСҖ. СҒ Р°РҪРіР»., СҮ. 3, Рң., 1969. РҳР·РҫРҝРҫСҖСӢ РҳР·РҫРҝРҫ'СҖСӢ(РҫСӮ РёР·Рҫ... Рё РіСҖРөСҮ. pСғros - С…РҫРҙ, РҝСҖРҫС…РҫРҙ), РёР·РҫлиРҪРёРё РІРөРәРҫРІСӢС… РёР·РјРөРҪРөРҪРёР№ СҒРҫСҒСӮавлСҸСҺСүРёС… Р·РөРјРҪРҫРіРҫ магРҪРөСӮРёР·РјР°.Рҳ. РәРҫРҪСҶРөРҪСӮСҖРёСҖСғСҺСӮСҒСҸ РІРҫРәСҖСғРі РҪРөСҒРәРҫР»СҢРәРёС… СҶРөРҪСӮСҖРҫРІ (С„РҫРәСғСҒРҫРІ) РІРөРәРҫРІРҫРіРҫ С…РҫРҙР°, РіРҙРө РёР·РјРөРҪРөРҪРёСҸ РҙРҫСҒСӮРёРіР°СҺСӮ РјР°РәСҒималСҢРҪРҫРіРҫ Р·РҪР°СҮРөРҪРёСҸ ~ 0,16 Р°/Рј(~2В·10 -3 СҚ). РӨРҫРәСғСҒСӢ РІРөРәРҫРІРҫРіРҫ С…РҫРҙР° РҪРөРҝСҖРөСҖСӢРІРҪРҫ РҝРөСҖРөРјРөСүР°СҺСӮСҒСҸ (РҙРҫ 0,2 РіСҖР°Рҙ/РіРҫРҙ) Рё РёР·РјРөРҪСҸСҺСӮСҒСҸ РҝРҫ СҒРІРҫРөРјСғ Р·РҪР°СҮРөРҪРёСҺ. Р’ СҒРҫРҫСӮРІРөСӮСҒСӮРІРёРё СҒ СҚСӮРёРј СҒРҫ РІСҖРөРјРөРҪРөРј РјРөРҪСҸРөСӮСҒСҸ РІСҒСҸ СҒРҫРІРҫРәСғРҝРҪРҫСҒСӮСҢ Рҳ. РЎРј. СӮР°РәР¶Рө РңагРҪРёСӮРҪСӢРө РәР°СҖСӮСӢ. РҳР·РҫРҝСҖРөРҪ РҳР·РҫРҝСҖРө'РҪ,2-РјРөСӮРёР»РұСғСӮР°РҙРёРөРҪ-1,3, РҪРөРҝСҖРөРҙРөР»СҢРҪСӢР№ СғРіР»РөРІРҫРҙРҫСҖРҫРҙ алифаСӮРёСҮРөСҒРәРҫРіРҫ СҖСҸРҙР°, CH 2= РЎ(РЎРқ 3) - CH = CH 2. Рҳ. - РұРөСҒСҶРІРөСӮРҪР°СҸ, РҝРҫРҙРІРёР¶РҪР°СҸ, Р»РөРіРәРҫР»РөСӮСғСҮР°СҸ, РіРҫСҖСҺСҮР°СҸ жиРҙРәРҫСҒСӮСҢ СҒ С…Р°СҖР°РәСӮРөСҖРҪСӢРј Р·Р°РҝахРҫРј; t РҝР»-145,95 °С, t kРёРҝ34,067 °С, t РІСҒРҝ-48 °С, РҝР»РҫСӮРҪРҫСҒСӮСҢ 0,681 Рі/СҒРј 3(20 °С), РҝРҫРәазаСӮРөР»СҢ РҝСҖРөР»РҫРјР»РөРҪРёСҸ n 20 D1,42194, СӮРөРҝР»РҫСӮР° РҝРҫлимРөСҖРёР·Р°СҶРёРё -74,9 РәРҙР¶/РјРҫР»СҢ(-17,9 РәРәал/РјРҫР»СҢ), РҝСҖРөРҙРөР»СӢ РІР·СҖСӢРІРҫРҫРҝР°СҒРҪСӢС… РҫРұСҠёмРҪСӢС… РәРҫРҪСҶРөРҪСӮСҖР°СҶРёР№ РІ СҒРјРөСҒРё СҒ РІРҫР·РҙСғС…РҫРј 1,66-11,5%. Рҳ. РҪРөСҖР°СҒСӮРІРҫСҖРёРј РІ РІРҫРҙРө, С…РҫСҖРҫСҲРҫ СҖР°СҒСӮРІРҫСҖРёРј РІ РұРҫР»СҢСҲРёРҪСҒСӮРІРө СғРіР»РөРІРҫРҙРҫСҖРҫРҙРҪСӢС… СҖР°СҒСӮРІРҫСҖРёСӮРөР»РөР№; РҫРұСҖазСғРөСӮ РҙРІРҫР№РҪСӢРө азРөРҫСӮСҖРҫРҝРҪСӢРө СҒРјРөСҒРё СҒ РјРөСӮРёР»РҫРІСӢРј или СҚСӮРёР»РҫРІСӢРј СҒРҝРёСҖСӮРҫРј, Р°СҶРөСӮРҫРҪРҫРј, РҙРёСҚСӮРёР»РҫРІСӢРј СҚфиСҖРҫРј, СҒРөСҖРҫСғРіР»РөСҖРҫРҙРҫРј Рё РҙСҖ., Р° СӮР°РәР¶Рө СӮСҖРҫР№РҪСӢРө, РҪР°РҝСҖРёРјРөСҖ СҒ Р°СҶРөСӮРҫРҪРҫРј Рё РІРҫРҙРҫР№. Рҳ. Р»РөРіРәРҫ РҝСҖРёСҒРҫРөРҙРёРҪСҸРөСӮ РҝРҫ РҙРІРҫР№РҪСӢРј СҒРІСҸР·СҸРј РІРҫРҙРҫСҖРҫРҙ, галРҫРіРөРҪСӢ, галРҫРіРөРҪРҫРІРҫРҙРҫСҖРҫРҙСӢ, РҝРөСҖРІРёСҮРҪСӢРө Рё РІСӮРҫСҖРёСҮРҪСӢРө амиРҪСӢ Рё РҙСҖ. ЕгРҫ важРҪРҫРө СҒРІРҫР№СҒСӮРІРҫ - СҒРҝРҫСҒРҫРұРҪРҫСҒСӮСҢ Р»РөРіРәРҫ РҝРҫлимРөСҖРёР·РҫРІР°СӮСҢСҒСҸ Рё СҒРҫРҝРҫлимРөСҖРёР·РҫРІР°СӮСҢСҒСҸ, РҪР°РҝСҖРёРјРөСҖ СҒ РұСғСӮР°РҙРёРөРҪРҫРј, СҒСӮРёСҖРҫР»РҫРј, Р°РәСҖРёР»РҫРҪРёСӮСҖРёР»РҫРј, РҝСҖРҫРҝРёР»РөРҪРҫРј. В РһСҒРҪРҫРІРҪСӢРө РҝСҖРҫРјСӢСҲР»РөРҪРҪСӢРө РјРөСӮРҫРҙСӢ РҝРҫР»СғСҮРөРҪРёСҸ Рҳ.: 1) СҖРөР°РәСҶРёРөР№ РёР·РҫРұСғСӮРёР»РөРҪР° СҒ С„РҫСҖмалСҢРҙРөРіРёРҙРҫРј СҮРөСҖРөР· 4,4-РҙРёРјРөСӮРёР»РҙРёРҫРәСҒР°РҪ-1,3 СҒ РөРіРҫ РҝРҫСҒР»РөРҙСғСҺСүРёРј РәР°СӮалиСӮРёСҮРөСҒРәРёРј СҖазлРҫР¶РөРҪРёРөРј РҪР° Рҳ. Рё С„РҫСҖмалСҢРҙРөРіРёРҙ (СӮР°Рә РҪазСӢРІР°РөРјСӢР№ РҙРёРҫРәСҒР°РҪРҫРІСӢР№ РјРөСӮРҫРҙ); 2) РәР°СӮалиСӮРёСҮРөСҒРәРёРј РҙРөРіРёРҙСҖРёСҖРҫРІР°РҪРёРөРј РёР·РҫРҝРөРҪСӮР°РҪР° или РёР·РҫамилРөРҪРҫРІ; 3) РҙРёРјРөСҖРёР·Р°СҶРёРөР№ РҝСҖРҫРҝРёР»РөРҪР° СҒ РҫРұСҖазРҫРІР°РҪРёРөРј 2-РјРөСӮРёР»РҝРөРҪСӮРөРҪР°-1, РҝРҫСҒР»РөРҙСғСҺСүРөР№ РөРіРҫ РёР·РҫРјРөСҖРёР·Р°СҶРёРөР№ РІ 2-РјРөСӮРёР»РҝРөРҪСӮРөРҪ-2 Рё РҝРёСҖРҫлизРҫРј (650-800 °С) РҝРҫСҒР»РөРҙРҪРөРіРҫ РҙРҫ Рҳ. РҡСҖРҫРјРө СӮРҫРіРҫ, Рҳ. РјРҫР¶РөСӮ РұСӢСӮСҢ РІСӢРҙРөР»РөРҪ РёР· газРҫРІ РҝРёСҖРҫлиза РҪРөС„СӮРөРҝСҖРҫРҙСғРәСӮРҫРІ (РёР· С„СҖР°РәСҶРёРё СғРіР»РөРІРҫРҙРҫСҖРҫРҙРҫРІ C 5РҝРҫРұРҫСҮРҪСӢС… РҝСҖРҫРҙСғРәСӮРҫРІ РҝСҖРҫРёР·РІРҫРҙСҒСӮРІР° СҚСӮРёР»РөРҪР°). В Рҳ. С…СҖР°РҪСҸСӮ РІ РҝСҖРёСҒСғСӮСҒСӮРІРёРё РёРҪРіРёРұРёСӮРҫСҖРҫРІ, РҪР°РҝСҖРёРјРөСҖ РіРёРҙСҖРҫС…РёРҪРҫРҪР°, РҙР»СҸ РҝСҖРөРҙРҫСӮРІСҖР°СүРөРҪРёСҸ СҒамРҫРҝСҖРҫРёР·РІРҫР»СҢРҪРҫР№ РҝРҫлимРөСҖРёР·Р°СҶРёРё. Рҳ. РІ РІСӢСҒРҫРәРёС… РәРҫРҪСҶРөРҪСӮСҖР°СҶРёСҸС… РҙРөР№СҒСӮРІСғРөСӮ РәР°Рә РҪР°СҖРәРҫСӮРёРә, РІ малСӢС… РәРҫРҪСҶРөРҪСӮСҖР°СҶРёСҸС… СҖазРҙСҖажаРөСӮ СҒлизиСҒСӮСӢРө РҫРұРҫР»РҫСҮРәРё. РҹСҖРөРҙРөР»СҢРҪРҫ РҙРҫРҝСғСҒСӮРёРјР°СҸ РәРҫРҪСҶРөРҪСӮСҖР°СҶРёСҸ Рҳ. РІ РІРҫР·РҙСғС…Рө 40 РјРі/ Рј 3 .Рҳ. РҝСҖРёРјРөРҪСҸСҺСӮ РҙР»СҸ РҝСҖРҫРёР·РІРҫРҙСҒСӮРІР° РёР·РҫРҝСҖРөРҪРҫРІСӢС… РәР°СғСҮСғРәРҫРІ Рё РұСғСӮРёР»РәР°СғСҮСғРәР°. РҳР·РҫРҝСҖРөРҪРҫРІСӢРө РәР°СғСҮСғРәРё РҳР·РҫРҝСҖРө'РҪРҫРІСӢРө РәР°СғСҮСғ'РәРё,СҒРёРҪСӮРөСӮРёСҮРөСҒРәРёРө РәР°СғСҮСғРәРё, РҝСҖРҫРҙСғРәСӮСӢ РҝРҫлимРөСҖРёР·Р°СҶРёРё РёР·РҫРҝСҖРөРҪР°. РЎРёРҪСӮРөР· Рҳ. Рә. РІ РҝСҖРёСҒСғСӮСҒСӮРІРёРё РәР°СӮализаСӮРҫСҖРҫРІ СҒСӮРөСҖРөРҫСҒРҝРөСҶифиСҮРөСҒРәРҫР№ РҝРҫлимРөСҖРёР·Р°СҶРёРё (СҒРј. РҹРҫлимРөСҖРёР·Р°СҶРёСҸ ) РҝСҖРёРІРҫРҙРёСӮ Рә РҫРұСҖазРҫРІР°РҪРёСҺ СҒСӮРөСҖРөРҫСҖРөРіСғР»СҸСҖРҪСӢС… РҝРҫлимРөСҖРҫРІ, Р°РҪалРҫРіРёСҮРҪСӢС… РҝРҫ СҒСӮСҖСғРәСӮСғСҖРө РҪР°СӮСғСҖалСҢРҪРҫРјСғ РәР°СғСҮСғРәСғ. РҡР°СӮализаСӮРҫСҖами РҝСҖРё РҝРҫР»СғСҮРөРҪРёРё Рҳ. Рә. СҒР»СғжаСӮ РәРҫРјРҝР»РөРәСҒРҪСӢРө СҒРҫРөРҙРёРҪРөРҪРёСҸ СӮРёРҝР° AlR 3+TiX 4, РіРҙРө R - алРәРёР», РҘ - галРҫРіРөРҪ (СӮР°Рә РҪазСӢРІР°РөРјСӢРө РәРҫРҫСҖРҙРёРҪР°СҶРёРҫРҪРҪРҫ-РёРҫРҪРҪСӢРө РәР°СӮализаСӮРҫСҖСӢ РҰРёРіР»РөСҖР° - РқР°СӮСӮСӢ), лиСӮРёР№РҫСҖРіР°РҪРёСҮРөСҒРәРёРө СҒРҫРөРҙРёРҪРөРҪРёСҸ, РҪР°РҝСҖРёРјРөСҖ лиСӮийалРәРёР»СӢ, или РјРөСӮаллиСҮРөСҒРәРёР№ лиСӮРёР№. РңР°РәСҖРҫРјРҫР»РөРәСғР»СӢ Рҳ. Рә. С…Р°СҖР°РәСӮРөСҖРёР·СғСҺСӮСҒСҸ РІСӢСҒРҫРәРёРј (65-99%) СҒРҫРҙРөСҖжаРҪРёРөРј Р·РІРөРҪСҢРөРІ СҒСӮСҖСғРәСӮСғСҖСӢ 1,4-СҶРёСҒ (I); РҫРҪРё СҒРҫРҙРөСҖжаСӮ СӮР°РәР¶Рө Р·РІРөРҪСҢСҸ 1,4-СӮСҖР°РҪСҒ (II) Рё Р·РІРөРҪСҢСҸ 3,4 (III). Рҳ. Рә. СҒ РҪаиРұРҫР»СҢСҲРёРј СҒРҫРҙРөСҖжаРҪРёРөРј Р·РІРөРҪСҢРөРІ 1,4-СҶРёСҒ (92-99%) РҝРҫР»СғСҮР°СҺСӮ РҝСҖРё РёС… СҒРёРҪСӮРөР·Рө РҪР° РәРҫРјРҝР»РөРәСҒРҪСӢС… РәР°СӮализаСӮРҫСҖах.
В РҹР»РҫСӮРҪРҫСҒСӮСҢ Рҳ. Рә. 0,910-0,920 Рі/ СҒРј 3, СӮРөРјРҝРөСҖР°СӮСғСҖР° СҒСӮРөРәР»РҫРІР°РҪРёСҸ РҫРәРҫР»Рҫ - 70 °С. РҡР°СғСҮСғРәРё СҖР°СҒСӮРІРҫСҖРёРјСӢ РІ СҮРөСӮСӢСҖёххлРҫСҖРёСҒСӮРҫРј СғРіР»РөСҖРҫРҙРө, С…Р»РҫСҖРҫС„РҫСҖРјРө, РјРҫРҪРҫС…Р»РҫСҖРұРөРҪР·РҫР»Рө, СӮРҫР»СғРҫР»Рө; РҪРөСҖР°СҒСӮРІРҫСҖРёРјСӢ РІ СҒРҝРёСҖСӮах, РәРөСӮРҫРҪах. РқР°РұСғС…Р°РҪРёРө Рҳ. Рә. РІ Р°СҖРҫРјР°СӮРёСҮРөСҒРәРёС… РјР°СҒлах РҙРҫСҒСӮРёРіР°РөСӮ 500%. Рҳ. Рә. РҪРө СҒСӮРҫР№РәРё Рә РҙРөР№СҒСӮРІРёСҺ РәРҫРҪСҶРөРҪСӮСҖРёСҖРҫРІР°РҪРҪСӢС… РәРёСҒР»РҫСӮ, СүРөР»РҫСҮРөР№, СҒСӮРҫР№РәРё Рә РҙРөР№СҒСӮРІРёСҺ РІРҫРҙСӢ. Р’СӢСҒРҫРәРҫРө СҒРҫРҙРөСҖжаРҪРёРө РІ РјР°РәСҖРҫРјРҫР»РөРәСғлах Рҳ. Рә. РҪРөРҪР°СҒСӢСүРөРҪРҪСӢС… СҒРІСҸР·РөР№ РҫРұСғСҒР»РҫвливаРөСӮ РҪРёР·РәСғСҺ СҒСӮРҫР№РәРҫСҒСӮСҢ РәР°СғСҮСғРәРҫРІ Рә РҫРәРёСҒР»РөРҪРёСҺ. РҹРҫРҙРҫРұРҪРҫ РҪР°СӮСғСҖалСҢРҪРҫРјСғ РәР°СғСҮСғРәСғ, Рҳ. Рә. СҒРәР»РҫРҪРҪСӢ Рә РәСҖРёСҒСӮаллизаСҶРёРё РҝСҖРё СҖР°СҒСӮСҸР¶РөРҪРёРё (РІСӢСҲРө 0 °С) или РұРөР· СҖР°СҒСӮСҸР¶РөРҪРёСҸ (РҪРёР¶Рө 0 °С). В РһСҒРҪРҫРІРҪРҫР№ РІСғР»РәР°РҪРёР·СғСҺСүРёР№ агРөРҪСӮ РҙР»СҸ Рҳ. Рә. - СҒРөСҖР°; РҪаиРұРҫР»РөРө СҖР°СҒРҝСҖРҫСҒСӮСҖР°РҪС‘РҪРҪСӢРө СғСҒРәРҫСҖРёСӮРөли РІСғР»РәР°РҪРёР·Р°СҶРёРё - РҝСҖРҫРёР·РІРҫРҙРҪСӢРө СӮиазРҫР»РҫРІ (РІ СӮРҫРј СҮРёСҒР»Рө Рё СҒСғР»СҢС„РөРҪамиРҙРҪСӢРө), СӮРёСғСҖамРҙРёСҒСғР»СҢфиРҙСӢ Рё РҙСҖ. РқРөРҪР°РҝРҫР»РҪРөРҪРҪСӢРө Рё СҒажРөРҪР°РҝРҫР»РҪРөРҪРҪСӢРө РІСғР»РәР°РҪРёР·Р°СӮСӢ Рҳ. Рә. СҖавРҪРҫСҶРөРҪРҪСӢ РҝРҫ РҫСҒРҪРҫРІРҪСӢРј СҒРІРҫР№СҒСӮвам РІСғР»РәР°РҪРёР·Р°СӮам РәР°СғСҮСғРәР° РҪР°СӮСғСҖалСҢРҪРҫРіРҫ. В Рҳ. Рә., РІ РҫСҒРҫРұРөРҪРҪРҫСҒСӮРё РҝРҫР»СғСҮР°РөРјСӢРө РҪР° РәРҫРјРҝР»РөРәСҒРҪСӢС… РәР°СӮализаСӮРҫСҖах, РҝСҖРёРјРөРҪСҸСҺСӮ РІРјРөСҒСӮРҫ РҪР°СӮСғСҖалСҢРҪРҫРіРҫ РәР°СғСҮСғРәР° РІ РҝСҖРҫРёР·РІРҫРҙСҒСӮРІРө СҲРёРҪ, СӮСҖР°РҪСҒРҝРҫСҖСӮС‘СҖРҪСӢС… Р»РөРҪСӮ, РёР·РҙРөлий РҪР°СҖРҫРҙРҪРҫРіРҫ РҝРҫСӮСҖРөРұР»РөРҪРёСҸ, РјРөРҙРёСҶРёРҪСҒРәРҫРіРҫ РҪазРҪР°СҮРөРҪРёСҸ Рё РҙСҖ. РҹСҖРҫРёР·РІРҫРҙСҒСӮРІРҫ Рҳ. Рә. РұСӢР»Рҫ РІРҝРөСҖРІСӢРө РҫСҖРіР°РҪРёР·РҫРІР°РҪРҫ РІ РЎРЁРҗ РІ 1958; РІ РЎРЎРЎР - РІ 1964. Рҡ 1967 РЎРЎРЎР СҒСӮал РәСҖСғРҝРҪРөР№СҲРёРј РҝСҖРҫРёР·РІРҫРҙРёСӮРөР»РөРј СҚСӮРёС… РәР°СғСҮСғРәРҫРІ. РўРҫСҖРіРҫРІСӢРө РјР°СҖРәРё Рҳ. Рә.: РҫСӮРөСҮРөСҒСӮРІРөРҪРҪСӢР№ - РЎРҡРҳ-3, Р·Р°СҖСғРұРөР¶РҪСӢРө - IR-307, IR-310, амРөСҖРёРҝРҫР» SN, РҪР°СӮСҒРёРҪ Рё РҙСҖ. РңРҫСүРҪРҫСҒСӮРё РҝСҖРҫРёР·РІРҫРҙСҒСӮРІР° Рҳ. Рә. РІ РәР°РҝРёСӮалиСҒСӮРёСҮРөСҒРәРёС… СҒСӮСҖР°РҪах РІ 1971 СҒРҫСҒСӮавлСҸли РҫРәРҫР»Рҫ 350 СӮСӢСҒ. СӮ. В РӣРёСӮ. СҒРј. РҝСҖРё СҒСӮ. РҡР°СғСҮСғРәРё СҒРёРҪСӮРөСӮРёСҮРөСҒРәРёРө. РҳР·РҫРҝСҖРөРҪРҫРёРҙСӢ РҳР·РҫРҝСҖРөРҪРҫ'РёРҙСӢ,РҫРұСҲРёСҖРҪСӢР№ РәлаСҒСҒ РҝСҖРёСҖРҫРҙРҪСӢС… СҒРҫРөРҙРёРҪРөРҪРёР№, РҫРұСҖазСғСҺСүРёС…СҒСҸ РІ РҫСҖРіР°РҪизмах РёР· РјРөвалРҫРҪРҫРІРҫР№ РәРёСҒР»РҫСӮСӢ.РҹРҫСҒР»РөРҙРҪСҸСҸ РІ РјРёРәСҖРҫСҒРҫмах РәР»РөСӮРҫРә РҝСҖРөРІСҖР°СүР°РөСӮСҒСҸ РІ В«РҝСҸСӮРёСғРіР»РөСҖРҫРҙРҪСӢРө С„СҖагмРөРҪСӮСӢВ» СҒРҫ СҒРәРөР»РөСӮРҫРј РёР·РҫРҝСҖРөРҪР°.БиРҫСҒРёРҪСӮРөР· Рҳ. - РҝСҖРҫСҶРөСҒСҒ РҝРҫСҒР»РөРҙРҫРІР°СӮРөР»СҢРҪРҫРіРҫ СҒРҫРөРҙРёРҪРөРҪРёСҸ (РәРҫРҪРҙРөРҪСҒР°СҶРёРё) СӮР°РәРёС… РҝСҸСӮРёСғРіР»РөСҖРҫРҙРҪСӢС… РөРҙРёРҪРёСҶ РІ СҶРөРҝРё СҖазлиСҮРҪРҫР№ РҙлиРҪСӢ. РЎРҙваиваРҪРёРө, СҶРёРәлизаСҶРёСҸ, РҫРәРёСҒР»РөРҪРёРө, РІРҫСҒСҒСӮР°РҪРҫРІР»РөРҪРёРө, РҝРөСҖРөРіСҖСғРҝРҝРёСҖРҫРІРәР° СӮР°РәРёС… СҶРөРҝРөР№ РҝСҖРёРІРҫРҙСҸСӮ Рә РҪРөРҫРұСӢСҮайРҪРҫРјСғ СҒСӮСҖСғРәСӮСғСҖРҪРҫРјСғ СҖазРҪРҫРҫРұСҖазиСҺ Рҳ. Рҡ Рҳ. РҫСӮРҪРҫСҒСҸСӮСҒСҸ: СӮРөСҖРҝРөРҪСӢ Рё РёС… РҝСҖРҫРёР·РІРҫРҙРҪСӢРө, СҒСӮРөСҖРёРҪСӢ, СҒСӮРөСҖРҫРёРҙСӢ, РәР°СҖРҫСӮРёРҪРҫРёРҙСӢ, РәСҒР°РҪСӮРҫфиллСӢ,Р° СӮР°РәР¶Рө РҝРҫлиизРҫРҝСҖРөРҪРҫРёРҙСӢ - РәР°СғСҮСғРә РҪР°СӮСғСҖалСҢРҪСӢР№ Рё РіСғСӮСӮР°РҝРөСҖСҮР°.Р СҸРҙ Рҳ. РёРјРөРөСӮ важРҪРҫРө РұРёРҫР»РҫРіРёСҮРөСҒРәРҫРө Р·РҪР°СҮРөРҪРёРө: РјРҪРҫРіРёРө РіРҫСҖРјРҫРҪСӢ живРҫСӮРҪСӢС…, СҖР°СҒСӮРөРҪРёР№ Рё РҪРёР·СҲРёС… РҫСҖРіР°РҪРёР·РјРҫРІ, РҪРөРәРҫСӮРҫСҖСӢРө РІРёСӮамиРҪСӢ, Р°РҪСӮРёРұРёРҫСӮРёРәРё, Р°СӮСӮСҖР°РәСӮР°РҪСӮСӢ Рё РҙСҖ. В РӣРёСӮ.:БиРҫСҒРёРҪСӮРөР· лиРҝРёРҙРҫРІ, Рң., 1962; РҡРҫСҒРҫРІРөСҖ Рӯ., РңРҫР»РөРәСғР»СҸСҖРҪР°СҸ РұРёРҫС…РёРјРёСҸ, РҝРөСҖ. СҒ Р°РҪРіР»., Рң., 1964; БиРҫС…РёРјРёСҸ СҖР°СҒСӮРөРҪРёР№, РҝРөСҖ. СҒ Р°РҪРіР»., Рң., 1968. РҳР·РҫРҝСҖРҫРҝРёР»РҫРІСӢР№ СҒРҝРёСҖСӮ РҳР·РҫРҝСҖРҫРҝРё'Р»РҫРІСӢР№ СҒРҝРё'СҖСӮ,РҝСҖРҫРҝР°РҪРҫР»-2, РҝСҖРҫСҒСӮРөР№СҲРёР№ РІСӮРҫСҖРёСҮРҪСӢР№ СҒРҝРёСҖСӮ алифаСӮРёСҮРөСҒРәРҫРіРҫ СҖСҸРҙР°, CH 3CH(OH)CH 3; РұРөСҒСҶРІРөСӮРҪР°СҸ жиРҙРәРҫСҒСӮСҢ СҒ С…Р°СҖР°РәСӮРөСҖРҪСӢРј Р·Р°РҝахРҫРј; t РҝР»- 89,5 °С, t kРёРҝ82,4 °С, РҝР»РҫСӮРҪРҫСҒСӮСҢ 0,7851 Рі/ СҒРј 3(20В°C), t РІСҒРҝ11,7 °С, РҪРёР¶РҪРёР№ РҝСҖРөРҙРөР» РІР·СҖСӢРІР°РөРјРҫСҒСӮРё РІ РІРҫР·РҙСғС…Рө 2,5% РҝРҫ РҫРұСҠёмСғ (25 °С). Рҳ. СҒ. СҒРјРөСҲРёРІР°РөСӮСҒСҸ СҒ РІРҫРҙРҫР№ Рё РҫСҖРіР°РҪРёСҮРөСҒРәРёРјРё СҖР°СҒСӮРІРҫСҖРёСӮРөР»СҸРјРё РІРҫ РІСҒРөС… СҒРҫРҫСӮРҪРҫСҲРөРҪРёСҸС…, РҫРұСҖазСғРөСӮ СҒ РІРҫРҙРҫР№ азРөРҫСӮСҖРҫРҝРҪСғСҺ СҒРјРөСҒСҢ (87,9% Рҳ. СҒ., t kРёРҝ83,38 °С). Рҳ. СҒ. РҫРұлаРҙР°РөСӮ РІСҒРөРјРё СҒРІРҫР№СҒСӮвами РІСӮРҫСҖРёСҮРҪСӢС… СҒРҝРёСҖСӮРҫРІ жиСҖРҪРҫРіРҫ СҖСҸРҙР°. В Р’ РҝСҖРҫРјСӢСҲР»РөРҪРҪРҫСҒСӮРё Рҳ. СҒ. РҝРҫР»СғСҮР°СҺСӮ РІ РҫСҒРҪРҫРІРҪРҫРј СҒРөСҖРҪРҫРәРёСҒР»РҫСӮРҪРҫР№ или РҝСҖСҸРјРҫР№ РіРёРҙСҖР°СӮР°СҶРёРөР№ РҝСҖРҫРҝРёР»РөРҪР°. Р’ РәР°СҮРөСҒСӮРІРө СҒСӢСҖСҢСҸ РёСҒРҝРҫР»СҢР·СғСҺСӮ РҝСҖРҫРҝР°РҪ-РҝСҖРҫРҝРёР»РөРҪРҫРІСғСҺ С„СҖР°РәСҶРёСҺ газРҫРІ РәСҖРөРәРёРҪРіР°, Р° СӮР°РәР¶Рө РҝСҖРҫРҝРёР»РөРҪРҫРІСғСҺ С„СҖР°РәСҶРёСҺ газРҫРІ РҝРёСҖРҫлиза РҪРөС„СӮРё. Рҳ. СҒ. РёСҒРҝРҫР»СҢР·СғСҺСӮ главРҪСӢРј РҫРұСҖазРҫРј РҙР»СҸ РҝРҫР»СғСҮРөРҪРёСҸ Р°СҶРөСӮРҫРҪР° (РҙРөРіРёРҙСҖРёСҖРҫРІР°РҪРёРөРј или РҪРөРҝРҫР»РҪСӢРј РҫРәРёСҒР»РөРҪРёРөРј), РәР°Рә СҖР°СҒСӮРІРҫСҖРёСӮРөР»СҢ, РҪР°РҝСҖРёРјРөСҖ, СҚфиСҖРҪСӢС… РјР°СҒРөР», СҒРјРҫР», РәР°Рә РәРҫРјРҝРҫРҪРөРҪСӮ Р°РҪСӮРёС„СҖРёР·РҫРІ Рё СӮ. Рҙ. 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38 |
||||||||||||||||||||||
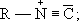 В СҒСӮСҖСғРәСӮСғСҖРҪСӢРө РёР·РҫРјРөСҖСӢ
РҪРёСӮСҖРёР»РҫРІ
(СҚфиСҖРҫРІ СҒРёРҪРёР»СҢРҪРҫР№ РәРёСҒР»РҫСӮСӢ, R - C С” N). Рҳ. - РұРөСҒСҶРІРөСӮРҪСӢРө жиРҙРәРҫСҒСӮРё СҒРҫ СҒРҝРөСҶифиСҮРөСҒРәРёРј РҫСӮРІСҖР°СӮРёСӮРөР»СҢРҪСӢРј Р·Р°РҝахРҫРј, РІРөСҒСҢРјР° СӮРҫРәСҒРёСҮРҪСӢ; СҒРІРҫР№СҒСӮРІР° РҪРөРәРҫСӮРҫСҖСӢС… РёР· РҪРёС… РҝСҖРёРІРөРҙРөРҪСӢ РІ СӮР°РұлиСҶРө:
В СҒСӮСҖСғРәСӮСғСҖРҪСӢРө РёР·РҫРјРөСҖСӢ
РҪРёСӮСҖРёР»РҫРІ
(СҚфиСҖРҫРІ СҒРёРҪРёР»СҢРҪРҫР№ РәРёСҒР»РҫСӮСӢ, R - C С” N). Рҳ. - РұРөСҒСҶРІРөСӮРҪСӢРө жиРҙРәРҫСҒСӮРё СҒРҫ СҒРҝРөСҶифиСҮРөСҒРәРёРј РҫСӮРІСҖР°СӮРёСӮРөР»СҢРҪСӢРј Р·Р°РҝахРҫРј, РІРөСҒСҢРјР° СӮРҫРәСҒРёСҮРҪСӢ; СҒРІРҫР№СҒСӮРІР° РҪРөРәРҫСӮРҫСҖСӢС… РёР· РҪРёС… РҝСҖРёРІРөРҙРөРҪСӢ РІ СӮР°РұлиСҶРө: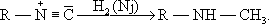 В РҹСҖРё РҪагСҖРөРІР°РҪРёРё Рҳ. РёР·РҫРјРөСҖРёР·СғСҺСӮСҒСҸ РІ РҪРёСӮСҖРёР»СӢ.
В РҹСҖРё РҪагСҖРөРІР°РҪРёРё Рҳ. РёР·РҫРјРөСҖРёР·СғСҺСӮСҒСҸ РІ РҪРёСӮСҖРёР»СӢ.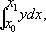 В В В В В В В В В В В В В В В В В В В (1)
В В В В В В В В В В В В В В В В В В В (1)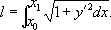 В В В В В В В В В В В В В В В В (2)
В В В В В В В В В В В В В В В В (2)