 |
|
Популярные авторы:: Борхес Хорхе Луис :: БСЭ :: Азимов Айзек :: Чехов Антон Павлович :: Горький Максим :: Станюкович Константин Михайлович :: Раззаков Федор :: Толстой Лев Николаевич :: Грин Александр :: Лесков Николай Семёнович Популярные книги:: Дюна (Книги 1-3) :: Утро космоса. Королев и Гагарин :: Крылатый человек :: Белые ночи :: Демон ростом два сантиметра :: Возвращение "Чайки" :: Пожиратель мух :: Ты, Марианна :: Истории тысячного года, или Приключения Тысячемуха, Початка и Недорода :: Карантин в Гранд-отеле |
Хирургия грыж брюшной стенкиModernLib.Net / Медицина / Воскресенский Николай Валерианович / Хирургия грыж брюшной стенки - Чтение (стр. 17)
Трудоспособность больных продолжает снижаться. При дальнейшем увеличении послеоперационных грыж, особенно располагающихся по белой линии и в области пупка, помимо увеличения грыжевого выпячивания, происходит значительное расхождение прямых мышц живота, еще большее истончение поверхности рубца; грыжевое выпячивание образует по нижнему своему краю отвисание и на резко выраженной складке и в окружности ее развиваются раздражение кожи, слущивание эпидермиса, воспалительные явления. При таких значительных изменениях передней брюшной стенки и органов брюшной полости, размещающихся в грыжевом выпячивании, вопрос об операции является уже весьма сложным. Техническая сложность операции делает прогноз сомнительным, особенно у больных пожилого возраста и тучных. При ущемлении послеоперационной грыжи операция еще более осложняется тем, что может потребоваться обширная резекция кишок, сальника. ПРОФИЛАКТИКА ПОСЛЕОПЕРАЦИОННЫХ ГРЫЖ И ЧАСТОТА ОТДЕЛЬНЫХ ВИДОВ ИХ Наиболее часто встречаются послеоперационные грыжи в правой подздошной области, иногда достигающие больших размеров. Причина их возникновения не только в тампонаде брюшной полости и вторичном, нередко длительном, заживлении раны при гнойных аппендицитах, но и в чрезмерной травме тканей стенки живота вследствие дополнительных разрезов для расширения доступа и в грубом растяжении крючками и зеркалами небольшой операционной раны. Никогда не следует делать попыток «обойтись» обязательно небольшими разрезами за счет чрезмерного растяжения краев раны, брюшины. Правильная оценка перед операцией возможных трудностей в связи с положением отростка, наличием инфильтрата, большой глубины раны у тучных больных, тяжести па-тологоанатомических изменений (сращения, перитонит) даст возможность выбрать соответствующий вид обезболивания и доступа. Немалое значение для уменьшения травматичности операции имеет и наличие второго ассистента[28]. Частота послеоперационных грыж после аппендэктомий колеблется в пределах 6—8 % (Н. 3. Монаков, А. П. Баженова). Близко к этим цифрам и число послеоперационных грыж после верхних срединных лапаротомий, а также после гинекологических операций. Наибольшее число послеоперационных грыж приходится на операции в правом подреберье. После операций на печени и желчных путях процент послеоперационных грыж достигает 14—15 (Мейо). Н. 3. Монаков объясняет это обстоятельство нефизиологичностью принятых разрезов брюшной стенки и закрытием операционной раны в основном за счет сшивания мышечных краев дефекта и предлагает для предупреждения образования послеоперационной грыжи «закрепить» пинию швов свободно пересаженным куском фасции. Следует еще учесть и то обстоятельство, что подавляющее число операций на желчных путях завершается тампонадой раны, нередко довольно обширной и длительной. Вопросы профилактики послеоперационных грыж связаны с правильным выбором разреза как в смысле свободного доступа к органам брюшной полости, так и его физиологич-ности. На VIII съезде российских хирургов этому вопросу были посвящены программные доклады и выступления (Н. М. Волкович, О. А. Юцевич, Н. И. Напалков, И. Н. Алексин-ский, И. К. Спижарный, В. М. Разумовский). Лучшими были признаны косо-переменный разрез для операций в правой подвздошной области и поперечный разрез при операциях больших пупочных и послеоперационных (вентральных) грыж. Н. М. Волкович в докладе на тему «Наиболее подходящий к нормальным условиям способ прохождения через брюшные стенки» подчеркнул, что «в основе операции должно быть возможно меньшее нарушение нормального строения брюшной стенки» и что преимущество надо отдавать ране, «приходящейся параллельно направлению волокон», поскольку при таких разрезах сосуды и нервы не повреждаются. Появившиеся в те годы предложения о поперечных лапаротомных разрезах брюшной стенки [13] не встретили принципиальных возражений участников съезда. Основные положения, выдвинутые на съезде, о лучших доступах через брюшную стенку в смысле профилактики послеоперационных грыж были впоследствии подтверждены рядом экспериментальных и клинических работ и остаются в силе и в настоящее время. В экспериментальной работе «О рациональных разрезах передней брюшной стенки для доступов к некоторым органам брюшной полости» Б. М. Рубашкин (1935) показал, что при косо-переменном разрезе по Волковичу—Дьяконову полностью сохраняются анатомо-физиологические особенности передней брюшной стенки, а спустя 13—25 дней восстанавливается мышечный тонус. Автор пришел к правильному выводу, что при тщательно проведенном строго по середине срединном лапаротомном разрезе «ни в какой мере не повреждаются нервы брюшной стенки». К этому выводу нужно прибавить, что в такой же степени важен и безупречный шов по средней линии. Следует все же сказать, что хотя разрез по Волковичу — Дьяконову и является наиболее физиологичным, однако он не всегда дает хороший доступ. На это в свое время указывал Н. И. Напалков. При расширении операционной раны приходится рассекать косые и поперечную мышцы, и в этих случаях возможность образования послеоперационной грыжи вполне реальна. Не лишен недостатков и менее распространенный у нас кулисный разрез Ленандера, при котором неизбежны, особенно в случае затрудненного доступа, повреждения сосудов и нервов, идущих к прямой мышце живота. Хотя именно «кулисность» разреза относится несомненно к преимуществам способа в смысле предупреждения возникновения послеоперационных грыж. В течение многих лет мы пользуемся при операциях на слепой кишке и червеобразном отростке вариантом кулисного разреза — косопараректальным разрезом. Разрез проводят справа через точку, лежащую на середине расстояния между верхней передней остью подвздошной кости и пупком, перпендикулярно к этой линии (рис. 101). Рассекают кожу, подкожную клетчатку с фасциями, переднюю стенку влагалища прямой мышцы живота; здесь необходимо отметить, что верхняя часть разреза несколько выходит за пределы влагалища прямой мышцы, однако это и является благоприятным моментом в предлагаемом доступе. В верхнем отделе разреза виден край прямой мышцы живота, ее осторожно отделяют и оттягивают в медиальную сторону. Таким образом, хирург во время операции не вынужден искать вслепую край прямой мышцы (как это делается при доступе по Ленандеру), чем достигается минимальная травма веточек межреберных нервов и самой мышцы. Благодаря тому что разрез имеет косое направление, стволы XI и XII межреберных нервов не повреждаются, они хорошо видны и их можно легко отодвинуть кверху и книзу. В самом верхнем углу раны видна задняя стенка влагалища прямой мышцы, на остальном же протяжении разреза предлежат только тонкая поперечная фасция и брюшина. Благодаря этому обстоятельству легко берется в широкую складку пристеночная брюшина (она как бы выпячивается «наружу» ниже дугласовой линии). В этом способе оперирования сохраняются все преимущества кулисного разреза Ленандера и устраняются его недостатки. Крупные сосуды, питающие переднюю брюшную стенку, как и при разрезе Ленандера, остаются вне разреза. Этот способ, примененный на большом количестве операций как при хроническом, так и при остром аппендиците, себя оправдал. Данный разрез, как и обычный параректальный, полностью позволяет расширить его вверх и вниз, не нарушая, однако, целости нервов и сосудов. Кроме того, при этом разрезе не приходится сильно растягивать рану крючками, что значительно уменьшает травму мышц и особенно брюшины и делает более простой операцию даже в трудных случаях. 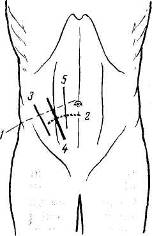 Рис. 101. Разрезы (доступы) при аппендэктомии (С. Л. Горелик и В. Ф. Парфентьева). 1 — linea spino-umbilicalis; 2 — linea semicircularis (Duglasi); 3 — разрез Волковича—Дьяконова; 4 — косо-параректальный разрез; 5 — разрез Ленандера. В профилактике послеоперационных грыж наряду с выбором доступа и атравматичным оперированием большую роль играет и тщательная асептика на всех этапах операции. Не следует при острых гнойных процессах одними и теми же инструментами (пинцеты, иглодержатели, крючки) работать и в глубине раны, и при зашивании брюшной стенки. Переходя от одного этапа вмешательства к другому (как при плановых операциях, так и при срочных), необходимо не только мыть руки сулемой или споласкивать их в тазу 0,25 % раствором нашатырного спирта, но и сменить инструменты и белье в окружности раны. При педантичном соблюдении правил асептики можно свести до минимума осложнения в ране и прежде всего нагноения. Гладкое заживление раны является одним из главных моментов в профилактике послеоперационных грыж. Следует также избегать тампонирования раны без соответствующих показаний. В деле предупреждения послеоперационных грыж не последнее место занимают предоперационная подготовка и ведение больных после операции[29]. Вопросы отпуска после различных операций на брюшной стенке в зависимости от условий труда и в соответствии со сложностью перенесенной операции, режима жизни и труда больных, а также вопросы трудоустройства в ближайшие месяцы после операции играют существенную роль в предупреждении послеоперационных грыж. ОПЕРАЦИИ ПРИ ПОСЛЕОПЕРАЦИОННЫХ ГРЫЖАХ «Хороши те способы, при которых производится по возможности меньшая дезорганизация передней брюшной стенки». Методы и способы операций при послеоперационных грыжах зависят от величины и локализации выпячивания, наличия спаек органов брюшной полости между собой и стенкой грыжевого мешка. Простое восстановление анатомических соотношений с последующим зашиванием брюшной стенки при небольших послеоперационных грыжах в ранние сроки в достаточной степени гарантирует благоприятный результат. Операция при больших длительно существующих грыжах, осложненных спаечным процессом, требует сложных восстановительных операций с дополнительными нередко вмешательствами по разделению спаек, рассечению рубцов, резекции кишечника и сальника. При больших реконструктивных операциях расширяются показания к применению аллопластических материалов с целью надежного закрытия больших дефектов передней стенки живота. При определении срока операции следует исходить из того обстоятельства, что развившаяся послеоперационная грыжа имеет тенденцию к постоянному увеличению и впоследствии к осложнениям (невправимость, ущемление, спаечная непроходимость кишок). Чем раньше сделана операция, тем меньше выражены изменения в тканях и органах, а само хирургическое вмешательство является менее сложным и более эффективным. При гладком течении и заживлении после первой операции можно оперировать послеоперационную грыжу спустя 6—8—10 месяцев в зависимости от вида и обширности первого вмешательства, общего состояния больного, величины и динамики роста грыжевого выпячивания. При склонности к ущемлению, а также при развивающемся синдроме спаечной непроходимости следует оперировать в возможно ранние сроки. Если в анамнезе есть указания на тяжело протекавший послеоперационный период в связи с обширным нагноением в ране, длительной тампонадой брюшной полости, тяжелой интоксикацией, перитонитом либо весьма длительным пребы-нием в стационаре по поводу релапаротомии, следует выждать больший срок, примерно 12—18 месяцев. На это время надо назначить больному определенный режим, принять меры к улучшению общего состояния, уменьшению страданий в связи с развитием спаечного процесса в грыжевом мешке и в брюшной полости. По показаниям следует рекомендовать ношение хорошо прилаженного бандажа. Показания к операции, особенно у пожилых, тучных больных или в случаях запущенных больших послеоперационных грыж, следует ставить продуманно, учитывая резистентность больного и опыт хирурга в восстановительных операциях. Небольшие послеоперационные грыжи лучше всего оперировать под местным обезболиванием по А. В. Вишневскому. При более сложных вмешательствах целесообразно пользоваться эфирно-кислородным масочным наркозом. Большие восстановительные операции, особенно после повторных рецидивов, лучше производить под поверхностным интубационным эфирно-кислородным наркозом с мышечными релаксантами. Операции по поводу послеоперационных грыж относятся к восстановительным, пластическим. В хирургии этих грыж применяются методы аутопластические, а л-лопластические и методы сочетанной (комбинированной) пластики дефектов брюшной стенки. Аутопластический метод «Пластику посредством живых тканей всегда нужно предпочитать вживанию нерассасывающихся инородных тел… При всякой пересадке лучше всего пользоваться тканями самого больного». Основным в восстановительной хирургии всегда являлся метод аутопластический — использование тканей больного, их перемещение, свободное или на ножке, с сохранением иннервации и кровообращения. Однако нельзя недоучитывать и то новое, современное, что внесло в восстановительную хирургию применение современных аллопластических материалов. Наш опыт основывается на сочетании аутопластического метода — использования местных тканей, даже и рубцово-измененных, — с аллопластическим. Аутопластика наиболее физиологична, так как основана на использовании биологически совместимых тканей. Однако не все виды аутопластики получили широкое распространение, ибо не все ткани легко приспосабливаются к новым условиям в случае нарушения их связей с материнской почвой. Менее капризны в этом отношении ткани невысокодифференциро-ванные, т.е. те, которые приживают в элементарных условиях питания и в то же время сохраняют способность регенерации при перенесении их в другое место того же организма. К таким тканях прежде всего относятся покровный эпителий (эпидермис), собственно кожа (без эпидермального слоя), фасция. Мышечная ткань при пересадке может быть использована лишь при сохранении достаточного кровоснабжения и иннервации, что исключает свободную пересадку мышечных лоскутов и делает довольно сложным перемещение их на широком основании или ножке с сохранением питающих сосудов и нервных ветвей. Следует отметить, что сторонниками мышечной пластики являлись в свое время видные хирурги нашей страны — С. Ф. Чиж, И. К. Спижарный, И. И. Греков, однако этот вид аутопластики не нашел распространения и в настоящее время к нему прибегают редко. Пересаженная для закрытия дефекта брюшной стенки мышца не будет иметь при активном сокращении брюшного пресса одновременного с остальными мышцами центрального импульса; это же обстоятельство будет иметь место и при рефлекторном сокращении брюшного пресса. Даже приживление лоскута не обусловливает сохранение его как мышечного органа; в дальнейшем мышца атрофируется и претерпевает соединительнотканное перерождение (А. И. Бакунин, В. М. Минц). Наиболее широкое распространение в практике восстановительных операций на брюшной стенке получила фас-циально-апоневротическая пластика, проверенная убедительными экспериментами и многочисленными клиническими наблюдениями [14]. Остин (Austin) с соавторами, Морзе (Morse) настоятельно рекомендуют пользоваться для прочного закрытия дефектов в брюшной стенке свободной фасциальной пластикой, предложенной еще В. А. Боголюбовым (1908), Киршнером (1909). Такого же мнения придерживаются Пик и Миллер (Реаск, Miller), которые вместе с Остином считают свободно взятую для восстановления брюшной стенки фасцию идеальным материалом. Фасциально — апоневротическая пластика Наибольшее распространение среди различных видов фасциально-апоневротической пластики получил способ удвоения апоневроза (дубликатура). Лучше всего при вентральных грыжах такое удвоение производить в поперечном направлении (по ходу волокон), что соответствует действию боковых мышц живота и натяжению фасциальных слоев (Н. М. Волкович, И. К. Спижарный, Н. И. Напалков). При небольших послеоперационных грыжах можно ограничиться послойной сепаровкой тканей, послойным их сшиванием после соответствующей обработки грыжевого мешка с завершением операции дубликатурой апоневроза (Grissn). Этот способ конструктивно прост и дает хорошие результаты (рис. 102). При более обширных и значительных изменениях в тканях, рубцовом перерождении в окружности грыжевых ворот целесообразно использовать в дубликатуре и рубцовые ткани, что уменьшит напряжение при удвоении апоневроза или мышечно-апоневротических слоев. При больших дефектах в стенке живота, когда дубли-катура слоев требует излишнего натяжения и создается опасность прорезывания швов, хорошую помощь неизменно оказывает аллопластическая прокладка из капроновой или тефлоновой сетки, на которой как бы монтируется дублика-тура без чрезмерного напряжения тканей. Такую прокладку можно имплантировать и из свободно взятого лоскута фасции (fascia lata). Что касается перемещения лоскута фасции на апоневротической или мышечно-апоневротической ножке, то такую пластику целесообразно применять в подходящих случаях при боковых послеоперационных грыжах в области пахового или бедренного канала (Н. И. Краковский, В. С. Степанов, П. Я. Ильченко) или при грыжах, расположенных не выше подвздошной области. 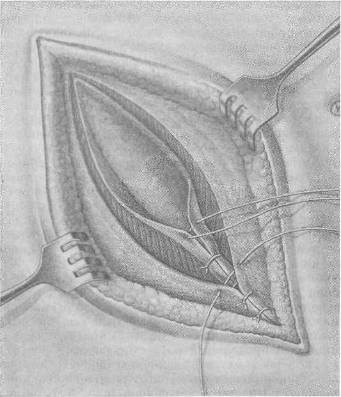 Рис. 102. Пластическое закрытие небольшой послеоперационной грыжи по Гриссону. Применение лоскутов широкой фасции бедра для закрытия дефектов брюшной стенки. Метод апоневротической аутопластики с использованием лоскутов из широкой фасции бедра, взятых свободно или на мышечно-апоневротической ножке, дает широкие возможности использования различных сочетаний для закрытия дефектов стенки живота (П. Г. Корнев, 1911; В. А. Перимов, 1912; А. Т. Лидский, 1926). Тщательная послойная сепаровка с сохранением и рубцово-измененных тканей (избыток их всегда легко иссечь на завершающем этапе пластики) помогает хорошо закрыть дефект, укрепив его дубликатурой апоневроза. В этой дубликатуре надо использовать, как уже указывалось, и рубцово-измененные участки апоневроза, что делает закрытие дефекта более прочным и дает возможность наложить два ряда швов без большого натяжения. Если дефект брюшной стенки велик и без значительного натяжения закрыть его не удается, следует прибегнуть к более сложным пластическим приемам, из которых наиболее доступным нужно считать перенесение и имплантацию свободного лоскута широкой фасции бедра. Аутофасция хорошо вживает и хотя впоследствии и претерпевает рубцовые изменения, она сохраняет функцию анатомически восстановленной ткани. Остин и соавторы, имеющие большой опыт в применении свободных лоскутов из широкой фасции бедра, считают, что свободно взятый трансплантат приживает во всяком случае не хуже, а может быть и лучше по сравнению с лоскутом на ножке. При свободной пересадке нет необходимости держать конечность согнутой до отделения ножки. Больной более активен, раньше встает с постели, что содействует процессам регенерации, приживлению. Техника пересадки фасции не очень сложна. После послойной отсепаровки тканей и выявления невозможности соединения их над дефектом без чрезмерного натяжения следует наложить ситуационные узловатые швы и выяснить размеры необходимого трансплантата. Затем проводят достаточно длинный продольный разрез на боковой поверхности бедра и иссекают нужной величины лоскут, который до использования помещают в теплый раствор новокаина или физиологический раствор поваренной соли. Фасцию и кожу на бедре зашивают. Если иссечен большой лоскут и края фасции не стягиваются швами, можно либо соединить их лишь в нескольких местах, либо использовать ослабляющие разрезы. Дефект после иссечения фасции даже без сшивания его краев хорошо выполняется плотной соединительной тканью (А. В. Старков, В. Р. Хесин, Н. И. Краковский), что предохраняет от развития мышечной грыжи. Перенесенный в дефект брюшной стенки лоскут фасции лучше расположить таким образом, чтобы он заходил под края дефекта на ширину 2—3 см. По краям дефекта лоскут следует подшить двухрядным узловатым или матрацным швом при умеренном натяжении. Отдельными швами осторожно можно прошить и подлежащие ткани, завязав эти швы над лоскутом на равном расстоянии друг от друга. Этим приемом удается ликвидировать свободные пространства между слоями сшиваемых тканей, что наряду с тщательным гемостазом является профилактикой сером. Кроме того, этим приемом нивелируется брюшное давление на основные швы по краям дефекта. Затем над прочно укрепленным имплантатом зашивают послойно ткани без чрезмерно частого наложения швов и лигатур. Полезно ввести в углы раны тонкие дренажи или длинные резиновые полоски. Повязка фиксируется клеолом и широкими поперечно наложенными полосками липкого пластыря. Тяжесть на область операции накладывают еще на операционном столе. На одной из наших операций закрытия дефекта брюшной стенки при послеоперационной рецидивной грыже лоскут широкой фасции бедра оказался слишком узким, неадекватным по своим размерам величине дефекта и при наложении ситуационных швов, фиксировавших лоскут к краям дефекта, натяжение оказалось чрезмерным. Остроконечным скальпелем были нанесены в шахматном порядке маленькие продольные разрезы по поверхности лоскута, который хорошо растянулся и был без натяжения прочно пришит к краям изъяна в стенке живота. Таким образом дефект был закрыт решетчатой фасциальной пластинкой. Последовало гладкое заживление. Морзе и др. применяли свободную пересадку лоскутов широкой фасции бедра для восстановления брюшной стенки при больших послеоперационных грыжах и пришли к заключению, что этот метод заслуживает большей популярности, так как всегда весьма эффективен. Различные мнения о судьбе фасциального лоскута, степени и характере его вживления имеют скорее академический, чем практический интерес. Как подчеркивают Пик и Миллер, свободно взятый лоскут аутофасции является хорошим материалом для восстановления брюшной стенки еще и потому, что он не способствует образованию спаек с органами брюшной полости, не травмирует их. После операций по поводу злокачественных новообразований имеет значение, что фасциальный лоскут не дает вторичного излучения, как танталовая сетка, и не является противопоказанием к проведению лучевой терапии. Наряду со свободной пересадкой многие хирурги охотно пользуются лоскутами широкой фасции из tractus iliotibialis, взятыми на апоневротической или мышечно-апоневротической ножке. Такими лоскутами успешно пользовались для закрытия грыжевых ворот при послеоперационных грыжах Н. И. Краковский, П. Я. Ильченко, В. С. Степанов, Остин и др. П. Я. Ильченко предлагает при больших срединных послеоперационных грыжах иссекать лоскуты фасции шириной 6—7 см, длиной до 35—38 см из продольных разрезов по наружной поверхности обоих бедер. Для того чтобы выделить хорошо васкуляризованную ножку из m. tensor fasciae latae, следует начать разрез на бедре на 2—3 см ниже spina iliaca anterior superior и окончить его не доходя примерно 6—8 см до уровня коленного сустава. Длинные лоскуты проводят корнцангом через образованные им подкожные тоннели и укладывают их диагонально таким образом, что перекрест их приходится над дефектом, соответственно которому получается удвоение фасциальных полос; последние по краям подшивают к краям дефекта; если остаются излишки лоскутов по длине, то их можно запрокинуть и пришить к краям дефекта и к месту перекреста лоскутов, благодаря чему создается прочное (тройное) закрытие изъяна в брюшной стенке. Могут применяться и другие варианты закрытия дефекта при помощи лоскутов широкой фасции бедра на ножке. В. С. Степанов пользуется более широкими лоскутами фасции. Остин и соавторы берут широкий лоскут с одного бедра, а с другого — более узкий для изготовления узких полосок (0,2—0,3 см), которые они применяют как шовный материал вместе с танталовыми швами (для наложения швов из аутофасции авторы пользуются иглой Мейо с длинным ушком). Н. 3. Монаков рекомендует закрывать дефект брюшной стенки при операции боковых послеоперационных грыж лоскутом на широком основании, взятым из стенки влагалища прямой мышцы на противоположной стороне. Из более сложных методов аутопластики с использованием тканей в окружности грыжевых ворот приводим описание конструктивной операции, предложенной Тропполи (Troppoli). Производится эллипсовидный разрез кожи, включающий старый рубец и измененные ткани. Левая рука отодвигает грыжевой мешок в сторону, доходя до края грыжевого кольца. Рука удерживается в этом положении и производится разрез жировой клетчатки отступив на 2 см от края кольца (рис. 103, а). Этот разрез доходит до апоневроза. Разрез в апоневрозе производится отступя на 1 см от медиального края (см. рис. 103, а). Указательный палец вводится под апоневроз через только что сделанный разрез, и апоневроз обычно легко приподнимается. Изогнутыми ножницами по пальцу разрезают апоневроз; палец располагается параллельно кольцу (рис. 103, б). Разрез апоневроза проводится не полностью вокруг кольца. Участок в 1,5 см шириной оставляется нетронутым на верхнем и нижнем краях (рис. 103, в). Далее края апоневроза сшиваются, при этом участок подкожного жира, покрывавшего грыжевое кольцо, переворачивается и превращается таким образом в предбрюшинный жир, покрывающий брюшину (рис. 103, г). После наложения первого и второго ряда швов на края апоневроза получается прочное закрытие грыжевых ворот (рис. 103, д). Операция по Тропполи показана лишь при срединных послеоперационных грыжах. Из других предложений следует кратко сказать об ослабляющих разрезах как способе закрытия мышечно-апоневротических дефектов стенки живота путем перемещения (сдвигания) апоневротических образований (A. Koontz, 1962) (рис. 104), а также о предложении 3. И. Карташева об использовании утильной фасции. 3. И. Карташев пользовался при операциях по поводу послеоперационных грыж консервированной фасцией как пластическим материалом. Лоскуты широкой фасции бедра, взятые от трупа, консервировались в течение 3—4 недель в глюкозо-пенициллиновой жидкости. Т. Д. Руиндеж отмечает большие пластические свойства таких лоскутов и их хорошую приживляемость, сообщая об успешных операциях у 28 больных, оперированных по поводу вентральных и рецидивных паховых грыж (1960). Кожная пластика Рен в 1914 г. опубликовал первые экспериментальные и клинические наблюдения над применением расщепленного кожного лоскута для аутопластики. Метод этот в пластической хирургии нашел свое дальнейшее развитие в многочисленных работах из клиник, руководимых Реном, Н. Н. Соколовым. Н. Н. Соколов назвал эту пластику «cutis-subcutis имплантация»[30]. Бетцнер (Batzner) определяет этот метод как пластику собственно кожей, лишенной эпидермального слоя, что больше всего соответствует сущности метода. Методом аутопластики, имплантацией кожи в глубину тканей (между отдельными слоями) в виде свободных лоскутов или взятых на ножке пользовались с успехом Г. Н. Булыгинский, С. Л. Тимофеев, И. Д. Корабельников. А. Н. Гостев успешно закрывал по этому способу большие дефекты брюшной стенки при послеоперационных грыжах. И. И. Греков сообщил об успешной операции «в своем буквально отчаянном случае с огромной рецидивирующей эвентрацией, который считали как „casus inoperabilis“ (H. H. Соколов). 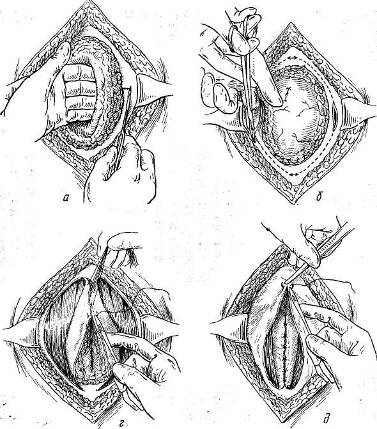 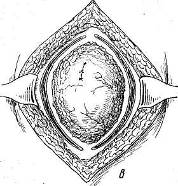 Рис. 103. Реконструкция брюшной стенки по Тропполи. 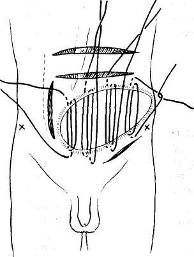  Рис. 104. Проведение ослабляющих разрезов на брюшной стенке, облегчающих наложение швов на обширный дефект (A. Koontz). Сторонники кожной пластики по Рену — Соколову считают этот метод лучшим для закрытия дефектов брюшной стенки, так как лоскут из собственно кожи хорошо вживает и трансформируется в прочную, васкуляризованную соединительнотканную пластину. Пластика требует для успешного исхода правильных показаний (операция не ранее 1—2 лет после первой операции, осложнившейся гнойным воспалением), тщательной подготовки и дефекта и донорского участка. Лоскут чаще всего берется с бедра, по его наружной или наружно-передней поверхности (рис. 105, а). В некоторых случаях при хорошем состоянии кожи в окружности дефекта можно произвести пластику расщепленным лоскутом на ножке. Удалять эпидермис следует до очерчивания лоскута специальным или ампутационным ножом при натяжении кожи. Глубина удаления эпидермоидного слоя определяется характерной беловатой сетчатой stratum reticulsum собственно кожи. Оставлять островки эпидермиса не следует, ибо из них могут образоваться впоследствии эпидермальные кисты. Снимание поверхностного слоя идет ровнее и быстрее, если придерживаться правила всегда делать сечение скальпелем по белесоватой полоске, получающейся при оттягивании эпидермиса на границе между ним и подлежащим ретикулярным слоем. Величина лоскута определяется размерами дефекта брюшной стенки. Лоскут собственно кожи берут после завершения первого этапа операции — отсепаровки тканей на брюшной стенке и определения величины дефекта, подлежащего пластическому закрытию. Затем лоскут на бедре очерчивают острым скальпелем, трансплантируют и пришивают к краям дефекта при сильном натяжении. Рен (рис. 105, б, в) подчеркивает, что лоскут при имплантации должен быть натянут, как кожа на барабане. Свенсон и Гаркинс (Swensn, Harkins) показали в эксперименте, что именно при таком натяжении оставшиеся, возможно, на лоскуте потовые и сальные железы атрофируются без образования кист. Операция завершается швами на подкожную клетчатку и кожу с последующим введением тонких дренажей в углы раны. Для успешности пересадки и профилактики инфекции необходимо тщательное соблюдение асептики, хорошая подготовка донорского участка. Для этого больной получает до операции в течение 3—4 дней теплую ванну. Накануне операции производят тщательное бритье донорского участка и закрывают его асептической повязкой или же повязкой с 40 % алкоголем (Рен). Непосредственно перед операцией кожу тщательно моют, обрабатывают эфиром и спиртом. 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20 |
|||||||