 |
|
Популярные авторы:: БСЭ :: Борхес Хорхе Луис :: Горький Максим :: Азимов Айзек :: Херберт Фрэнк :: Чехов Антон Павлович :: Раззаков Федор :: Толстой Лев Николаевич :: Грин Александр :: Астафьев Виктор Петрович Популярные книги:: Дюна (Книги 1-3) :: The Boarding House :: Три цвета времени :: Упражнения по стилистике русского языка :: Преодоление :: Талисман из Рэдволла :: Плацдарм :: Закрой рот, джинн – кишки простудишь… :: Авантюристка :: Андропов. 7 тайн генсека с Лубянки |
Большая Советская Энциклопедия (ЖЕ)ModernLib.Net / Энциклопедии / БСЭ / Большая Советская Энциклопедия (ЖЕ) - Чтение (стр. 13)
В Р–. Рҝ. СғСҒРҝРөСҲРҪРҫ СҖазвиваРөСӮСҒСҸ Рё РІ РҙСҖ. СҒРҫСҶиалиСҒСӮРёСҮРөСҒРәРёС… СҒСӮСҖР°РҪах. РңРөСҒСӮРҫСҖРҫР¶РҙРөРҪРёСҸ Р¶РөР»РөР·РҪРҫР№ СҖСғРҙСӢ РёРјРөСҺСӮСҒСҸ РІ РҹРҫР»СҢСҲРө, Р СғРјСӢРҪРёРё, Р§РөС…РҫСҒР»РҫРІР°РәРёРё. Р—Р°РҝР°СҒСӢ РөС‘ РІ Р‘РҫлгаСҖРёРё Рё Р’РөРҪРіСҖРёРё РҪРөР·РҪР°СҮРёСӮРөР»СҢРҪСӢ. Р§РөС…РҫСҒР»РҫРІР°РәРёСҸ, Р’РөРҪРіСҖРёСҸ, Р СғРјСӢРҪРёСҸ, ГДР, СҮР°СҒСӮРёСҮРҪРҫ РҹРҫР»СҢСҲР° РёРјРҝРҫСҖСӮРёСҖСғСҺСӮ Р¶РөР»РөР·РҪСғСҺ СҖСғРҙСғ. РҡРёСӮай РұРҫРіР°СӮ Р¶РөР»РөР·РҪСӢРјРё СҖСғРҙами, РәРҫСӮРҫСҖСӢРө СҖазмРөСүРөРҪСӢ РІРҫ РјРҪРҫРіРёС… РҝСҖРҫРІРёРҪСҶРёСҸС…, РҫСҒРҫРұРөРҪРҪРҫ РҪР° РЎ.-Р’. СҒСӮСҖР°РҪСӢ. В Р–. Рҝ. РәР°РҝРёСӮалиСҒСӮРёСҮРөСҒРәРёС… СҒСӮСҖР°РҪ С…Р°СҖР°РәСӮРөСҖРёР·СғРөСӮСҒСҸ РҪРөСҒРҫРҫСӮРІРөСӮСҒСӮРІРёРөРј РјРөР¶РҙСғ Р·Р°РҝР°СҒами, РҙРҫРұСӢСҮРөР№ Рё РҝРҫСӮСҖРөРұР»РөРҪРёРөРј СҖСғРҙ. Р‘РҫР»СҢСҲРёРө СҖРөСҒСғСҖСҒСӢ СҖСғРҙ РёРјРөСҺСӮ СҒСӮСҖР°РҪСӢ СҒРҫ СҒлаРұРҫСҖазвиСӮРҫР№ РјРөСӮаллСғСҖРіРёСҮРөСҒРәРҫР№ РҝСҖРҫРјСӢСҲР»РөРҪРҪРҫСҒСӮСҢСҺ. 3/ 4Р·Р°РҝР°СҒРҫРІ Р¶РөР»РөР·РҪРҫР№ СҖСғРҙСӢ РәР°РҝРёСӮалиСҒСӮРёСҮРөСҒРәРҫРіРҫ РјРёСҖР° СҒРҫСҒСҖРөРҙРҫСӮРҫСҮРөРҪРҫ РІ 4 СҒСӮСҖР°РҪах - Р‘СҖазилии, РҡР°РҪР°РҙРө, РҳРҪРҙРёРё Рё РҗРІСҒСӮСҖалии. РһРұСүРёРө Р·Р°РҝР°СҒСӢ Р¶РөР»РөР·РҪСӢС… СҖСғРҙ РЎРЁРҗ РҫСҶРөРҪРёРІР°СҺСӮСҒСҸ РІ 10 РјР»СҖРҙ. СӮ(СҒ СҒРҫРҙРөСҖжаРҪРёРөРј Р¶РөР»РөР·Р° РҫРәРҫР»Рҫ 60%). Р—Р°РҝР°СҒСӢ РұРҫРіР°СӮСӢС… СҖСғРҙ Р’РөСҖС…РҪРөРіРҫ РҫР·РөСҖР° (РҫСҒРҪРҫРІРҪРҫР№ СҖСғРҙРҪРҫР№ РұазСӢ РЎРЁРҗ) - 1,1 РјР»СҖРҙ. СӮ.РһРәРҫР»Рҫ 90% СҖСғРҙСӢ РҙРҫРұСӢРІР°РөСӮСҒСҸ РҫСӮРәСҖСӢСӮСӢРј СҒРҝРҫСҒРҫРұРҫРј. Р’ СҒРІСҸР·Рё СҒ СғРјРөРҪСҢСҲРөРҪРёРөРј Р·Р°РҝР°СҒРҫРІ РұРҫРіР°СӮСӢС… СҖСғРҙ РјРҪРҫРіРҫ РІРҪРёРјР°РҪРёСҸ СғРҙРөР»СҸРөСӮСҒСҸ РёСҒРҝРҫР»СҢР·РҫРІР°РҪРёСҺ РұРөРҙРҪСӢС… СҖСғРҙ (СӮР°РәРҫРҪРёСӮРҫРІ). Р’ 1969 РІ РЎРЁРҗ РҙРҫРұСӢСӮ 91 РјР»РҪ. СӮРё РёРјРҝРҫСҖСӮРёСҖРҫРІР°РҪРҫ 40 РјР»РҪ. СӮСӮРҫРІР°СҖРҪРҫР№ Р¶РөР»РөР·РҪРҫР№ СҖСғРҙСӢ. РӨСҖР°РҪСҶРёСҸ РҫРұлаРҙР°РөСӮ РҪаиРұРҫР»РөРө РәСҖСғРҝРҪСӢРј РІ Р—Р°РҝР°РҙРҪРҫР№ ЕвСҖРҫРҝРө РӣРҫСӮР°СҖРёРҪРіСҒРәРёРј РјРөСҒСӮРҫСҖРҫР¶РҙРөРҪРёРөРј Р¶РөР»РөР·РҪСӢС… СҖСғРҙ СҒ РҫРұСүРёРјРё Р·Р°РҝР°СҒами 7,1 РјР»СҖРҙ. СӮ,РІ СӮРҫРј СҮРёСҒР»Рө РҙРҫСҒСӮРҫРІРөСҖРҪСӢРө Рё РІРөСҖРҫСҸСӮРҪСӢРө 4,5 РјР»СҖРҙ. СӮ(СҒ СҒРҫРҙРөСҖжаРҪРёРөРј Р¶РөР»РөР·Р° 30%). Р’ 1969 РҙРҫРұСӢСӮРҫ 56 РјР»РҪ. СӮРё СҚРәСҒРҝРҫСҖСӮРёСҖРҫРІР°РҪРҫ 19 РјР»РҪ. СӮСӮРҫРІР°СҖРҪРҫР№ СҖСғРҙСӢ. РЁРІРөСҶРёСҸ РҝРҫ РҙРҫРұСӢСҮРө Р¶РөР»РөР·РҪРҫР№ СҖСғРҙСӢ Р·Р°РҪРёРјР°РөСӮ СҒСҖРөРҙРё РәР°РҝРёСӮалиСҒСӮРёСҮРөСҒРәРёС… СҒСӮСҖР°РҪ ЕвСҖРҫРҝСӢ 2-Рө РјРөСҒСӮРҫ (РҝРҫСҒР»Рө РӨСҖР°РҪСҶРёРё). Р—Р°РҝР°СҒСӢ РөС‘ РұРҫРіР°СӮСӢС… СҖСғРҙ РёСҒСҮРёСҒР»СҸСҺСӮСҒСҸ РІ 2,4 РјР»СҖРҙ. СӮ.Р’ 1969 РҙРҫРұСӢСӮРҫ 30 РјР»РҪ. СӮ,СҚРәСҒРҝРҫСҖСӮРёСҖРҫРІР°РҪРҫ 28 РјР»РҪ. СӮ.Р—Р°РҝР°СҒСӢ Р¶РөР»РөР·РҪСӢС… СҖСғРҙ РҳРҪРҙРёРё РҙРҫСҒСӮРёРіР°СҺСӮ 22 РјР»СҖРҙ. СӮ.Р СғРҙР° РҙРҫРұСӢРІР°РөСӮСҒСҸ РҫСӮРәСҖСӢСӮСӢРј СҒРҝРҫСҒРҫРұРҫРј. Р’ 1969 РҙРҫРұСӢСӮРҫ 30 РјР»РҪ. СӮ,СҚРәСҒРҝРҫСҖСӮРёСҖРҫРІР°РҪРҫ 19 РјР»РҪ. СӮ.БалаРҪСҒРҫРІСӢРө Р·Р°РҝР°СҒСӢ СҖСғРҙ Р‘СҖазилии РҫСҶРөРҪРёРІР°СҺСӮСҒСҸ РІ 16,5 РјР»СҖРҙ. СӮ(СҒРҫРҙРөСҖжаРҪРёРө Р¶РөР»РөР·Р° РҫСӮ 50 РҙРҫ 66%). Р’ 1969 РҙРҫРұСӢСӮРҫ 27 РјР»РҪ. СӮСҖСғРҙСӢ Рё СҚРәСҒРҝРҫСҖСӮРёСҖРҫРІР°РҪРҫ 18 РјР»РҪ. СӮ.Р—РҪР°СҮРёСӮ, Р·Р°РҝР°СҒами РұРҫРіР°СӮСӢС… СҖСғРҙ РҫРұлаРҙР°РөСӮ РҡР°РҪР°РҙР°, РіРҙРө РІ 1969 РҙРҫРұСӢСӮРҫ 38 РјР»РҪ. СӮРё СҚРәСҒРҝРҫСҖСӮРёСҖРҫРІР°РҪРҫ 32 РјР»РҪ. СӮ(главРҪСӢРј РҫРұСҖазРҫРј РІ РЎРЁРҗ). Р’ 1969 РҙРҫРұСӢСӮРҫ (РјР»РҪ. СӮСҖСғРҙСӢ): РІ РҗРІСҒСӮСҖалии 32, РӣРёРұРөСҖРёРё 24, Р’РөРҪРөСҒСғСҚР»Рө 19, Чили 12. Р’РөлиРәРҫРұСҖРёСӮР°РҪРёСҸ, РӨР Р“, РҳСӮалиСҸ, РҜРҝРҫРҪРёСҸ РҪРө РҫРұлаРҙР°СҺСӮ РҙРҫСҒСӮР°СӮРҫСҮРҪСӢРјРё Р·Р°РҝР°СҒами РұРҫРіР°СӮСӢС… Р¶РөР»РөР·РҪСӢС… СҖСғРҙ. РһРҪРё СғРҙРҫРІР»РөСӮРІРҫСҖСҸСҺСӮ СҒРІРҫРё РҝРҫСӮСҖРөРұРҪРҫСҒСӮРё Р·Р° СҒСҮС‘СӮ РҙРҫРұСӢСҮРё РұРөРҙРҪСӢС… СҖСғРҙ Рё РёРјРҝРҫСҖСӮР° РұРҫРіР°СӮСӢС… СҖСғРҙ. В РӣРёСӮ.:Р–РөР»РөР·РҫСҖСғРҙРҪР°СҸ Рұаза СҮРөСҖРҪРҫР№ РјРөСӮаллСғСҖРіРёРё РЎРЎРЎР , Рң., 1957; Р§РөСҖРҪР°СҸ РјРөСӮаллСғСҖРіРёСҸ РәР°РҝРёСӮалиСҒСӮРёСҮРөСҒРәРёС… СҒСӮСҖР°РҪ, СҮ. 7 - Р–РөР»РөР·РҫСҖСғРҙРҪР°СҸ РҝСҖРҫРјСӢСҲР»РөРҪРҪРҫСҒСӮСҢ Рё РҫРұРҫРіР°СүРөРҪРёРө СҖСғРҙ, Рң., 1960; РўРөС…РҪРёСҮРөСҒРәРёР№ РҝСҖРҫРіСҖРөСҒСҒ РІ СҮРөСҖРҪРҫР№ РјРөСӮаллСғСҖРіРёРё РЎРЎРЎР . Р–РөР»РөР·РҫСҖСғРҙРҪР°СҸ РҝСҖРҫРјСӢСҲР»РөРҪРҪРҫСҒСӮСҢ, Рң., 1962; Р‘СӢС…РҫРІРөСҖ Рқ. Рҗ., РӯРәРҫРҪРҫРјРёРәР° РјРёРҪРөСҖалСҢРҪРҫРіРҫ СҒСӢСҖСҢСҸ. Р–РөР»РөР·Рҫ, Рң., 1967; Р‘СҖР°СғРҪ Р“. Рҗ., Р–РөР»РөР·РҫСҖСғРҙРҪР°СҸ Рұаза СҮРөСҖРҪРҫР№ РјРөСӮаллСғСҖРіРёРё РЎРЎРЎР , 2 РёР·Рҙ., Рң., 1970; РЎР»РөРҙР·СҺРә Рҹ. Р•., РһРұ СғР»СғСҮСҲРөРҪРёРё РёСҒРҝРҫР»СҢР·РҫРІР°РҪРёСҸ СҖРөР·РөСҖРІРҫРІ РҝСҖРҫРёР·РІРҫРҙСҒСӮРІР° РІ Р¶РөР»РөР·РҫСҖСғРҙРҪРҫР№ РҝСҖРҫРјСӢСҲР»РөРҪРҪРҫСҒСӮРё, «ГРҫСҖРҪСӢР№ Р¶СғСҖРҪал», 1970, в„– 7; Р’РёРҪРҫРіСҖР°РҙРҫРІ B. РЎ., Р“РҫСҖРҪРҫРҙРҫРұСӢРІР°СҺСүР°СҸ РҝСҖРҫРјСӢСҲР»РөРҪРҪРҫСҒСӮСҢ СҮРөСҖРҪРҫР№ РјРөСӮаллСғСҖРіРёРё Рә XXIV СҒСҠРөР·РҙСғ РҡРҹРЎРЎ, СӮам Р¶Рө, 1971, в„– 3. В Р’. Рҗ. РҗРҙамСҮСғРә. Р–РөР»РөР·РҫСҒРёРҪРөСҖРҫРҙРёСҒСӮСӢР№ Рәалий Р–РөР»РөР·РҫСҒРёРҪРөСҖРҫ'РҙРёСҒСӮСӢР№ РәР°'лий,K 3[Fe(CN) 6], СӮРҫ Р¶Рө, СҮСӮРҫ РәСҖР°СҒРҪР°СҸ РәСҖРҫРІСҸРҪР°СҸ СҒРҫР»СҢ, или РҡалиСҸ РіРөРәСҒР°СҶРёР°РҪРҫС„РөСҖСҖРёР°СӮ . Р–РөР»РөР·РҫСғРіР»РөСҖРҫРҙРёСҒСӮСӢРө СҒРҝлавСӢ Р–РөР»РөР·РҫСғРіР»РөСҖРҫ'РҙРёСҒСӮСӢРө СҒРҝла'РІСӢ,СҒРҝлавСӢ Р¶РөР»РөР·Р° СҒ СғРіР»РөСҖРҫРҙРҫРј РҪР° РҫСҒРҪРҫРІРө Р¶РөР»РөР·Р°. Р’Р°СҖСҢРёСҖСғСҸ СҒРҫСҒСӮав Рё СҒСӮСҖСғРәСӮСғСҖСғ, РҝРҫР»СғСҮР°СҺСӮ Р–. СҒ. СҒ СҖазРҪРҫРҫРұСҖазРҪСӢРјРё СҒРІРҫР№СҒСӮвами, СҮСӮРҫ РҙРөлаРөСӮ РёС… СғРҪРёРІРөСҖСҒалСҢРҪСӢРјРё РјР°СӮРөСҖиалами. РазлиСҮР°СҺСӮ СҮРёСҒСӮСӢРө Р–. СҒ. (СҒРҫ СҒР»РөРҙами РҝСҖРёРјРөСҒРөР№), РҝРҫР»СғСҮР°РөРјСӢРө РІ РҪРөРұРҫР»СҢСҲРёС… РәРҫлиСҮРөСҒСӮвах РҙР»СҸ РёСҒСҒР»РөРҙРҫРІР°СӮРөР»СҢСҒРәРёС… СҶРөР»РөР№, Рё СӮРөС…РҪРёСҮРөСҒРәРёРө Р–. СҒ. - СҒСӮали (РҙРҫ 2%РЎ) Рё СҮСғРіСғРҪСӢ (СҒРІ. 2% РЎ), РјРёСҖРҫРІРҫРө РҝСҖРҫРёР·РІРҫРҙСҒСӮРІРҫ РәРҫСӮРҫСҖСӢС… РёР·РјРөСҖСҸРөСӮСҒСҸ СҒРҫСӮРҪСҸРјРё РјР»РҪ. СӮ.РўРөС…РҪРёСҮРөСҒРәРёРө Р–. СҒ. СҒРҫРҙРөСҖжаСӮ РҝСҖРёРјРөСҒРё. РҳС… РҙРөР»СҸСӮ РҪР° РҫРұСӢСҮРҪСӢРө (С„РҫСҒС„РҫСҖ Р , СҒРөСҖР° S, РјР°СҖРіР°РҪРөСҶ Mn, РәСҖРөРјРҪРёР№ Si, РІРҫРҙРҫСҖРҫРҙ Рқ, азРҫСӮ N, РәРёСҒР»РҫСҖРҫРҙ Рһ), Р»РөРіРёСҖСғСҺСүРёРө (С…СҖРҫРј Cr, РҪРёРәРөР»СҢ Ni, РјРҫлиРұРҙРөРҪ Mo, РІРҫР»СҢС„СҖам W, РІР°РҪР°РҙРёР№ V, СӮРёСӮР°РҪ Ti, РәРҫРұалСҢСӮ РЎРҫ, РјРөРҙСҢ Cu Рё РҙСҖ.) Рё РјРҫРҙифиСҶРёСҖСғСҺСүРёРө (магРҪРёР№ Mg, СҶРөСҖРёР№ Ce, РәалСҢСҶРёР№ Ca Рё РҙСҖ.). Р’ РұРҫР»СҢСҲРёРҪСҒСӮРІРө СҒР»СғСҮР°РөРІ РҫСҒРҪРҫРІРҫР№, РҫРҝСҖРөРҙРөР»СҸСҺСүРөР№ СҒСӮСҖРҫРөРҪРёРө Рё СҒРІРҫР№СҒСӮРІР° СҒСӮалРөР№ Рё СҮСғРіСғРҪРҫРІ, СҸРІР»СҸРөСӮСҒСҸ СҒРёСҒСӮРөРјР° Fe - РЎ. РқР°СҮалРҫ РҪР°СғСҮРҪРҫРјСғ РёР·СғСҮРөРҪРёСҺ СҚСӮРҫР№ СҒРёСҒСӮРөРјСӢ РҝРҫР»Рҫжили СҖСғСҒСҒРәРёРө РјРөСӮаллСғСҖРіРё Рҹ. Рҹ. РҗРҪРҫСҒРҫРІ (1831) Рё Р”. Рҡ. Р§РөСҖРҪРҫРІ (1868). РҗРҪРҫСҒРҫРІ РІРҝРөСҖРІСӢРө РҝСҖРёРјРөРҪРёР» РјРёРәСҖРҫСҒРәРҫРҝ РҝСҖРё РёСҒСҒР»РөРҙРҫРІР°РҪРёРё Р–. СҒ., Р° Р§РөСҖРҪРҫРІ СғСҒСӮР°РҪРҫРІРёР» РёС… РәСҖРёСҒСӮаллиСҮРөСҒРәСғСҺ РҝСҖРёСҖРҫРҙСғ, РҫРұРҪР°СҖСғжил РҙРөРҪРҙСҖРёСӮРҪСғСҺ РәСҖРёСҒСӮаллизаСҶРёСҺ Рё РҫСӮРәСҖСӢР» РІ РҪРёС… РҝСҖРөРІСҖР°СүРөРҪРёСҸ РІ СӮРІС‘СҖРҙРҫРј СҒРҫСҒСӮРҫСҸРҪРёРё. РҳР· Р·Р°СҖСғРұРөР¶РҪСӢС… СғСҮС‘РҪСӢС…, СҒРҝРҫСҒРҫРұСҒСӮРІРҫвавСҲРёС… СҒРҫР·РҙР°РҪРёСҺ РҙиагСҖаммСӢ СҒРҫСҒСӮРҫСҸРҪРёСҸ Fe - РЎ СҒРҝлавРҫРІ, СҒР»РөРҙСғРөСӮ РҫСӮРјРөСӮРёСӮСҢ РӨ. РһСҒРјРҫРҪРҙР° (РӨСҖР°РҪСҶРёСҸ), РЈ. Р§. Р РҫРұРөСҖСӮСҒР°-РһСҒСӮРөРҪР° (РҗРҪглиСҸ), Р‘. Р РҫР·РөРұРҫРјР° (Р“РҫллаРҪРҙРёСҸ) Рё Рҹ. Р“РөСҖРөРҪСҒР° (Р“РөСҖРјР°РҪРёСҸ). В РӨазРҫРІСӢРө СҒРҫСҒСӮРҫСҸРҪРёСҸ Р–. СҒ.РҝСҖРё СҖазРҪСӢС… СҒРҫСҒСӮавах Рё СӮРөРјРҝРөСҖР°СӮСғСҖах РҫРҝРёСҒСӢРІР°СҺСӮСҒСҸ РҙиагСҖаммами СҒСӮР°РұРёР»СҢРҪРҫРіРҫ ( СҖРёСҒ. 1 , Р°) Рё РјРөСӮР°СҒСӮР°РұРёР»СҢРҪРҫРіРҫ ( СҖРёСҒ. 1 , Рұ) СҖавРҪРҫРІРөСҒРёР№. Р’ СҒСӮР°РұРёР»СҢРҪРҫРј СҒРҫСҒСӮРҫСҸРҪРёРё РІ Р–. СҒ. РІСҒСӮСҖРөСҮР°СҺСӮСҒСҸ жиРҙРәРёР№ СҖР°СҒСӮРІРҫСҖ СғРіР»РөСҖРҫРҙР° РІ Р¶РөР»РөР·Рө (Р–), СӮСҖРё СӮРІС‘СҖРҙСӢС… СҖР°СҒСӮРІРҫСҖР° СғРіР»РөСҖРҫРҙР° РІ РҝРҫлимРҫСҖС„РҪСӢС… РјРҫРҙифиРәР°СҶРёСҸС… Р¶РөР»РөР·Р° (СӮР°РұР». 1) В РўР°РұР». 1.- РҡСҖРёСҒСӮаллиСҮРөСҒРәРёРө фазСӢ Р¶РөР»РөР·РҫСғРіР»РөСҖРҫРҙРёСҒСӮСӢС… СҒРҝлавРҫРІ
a-СҖР°СҒСӮРІРҫСҖ (a-С„РөСҖСҖРёСӮ), g-СҖР°СҒСӮРІРҫСҖ (Р°СғСҒСӮРөРҪРёСӮ) Рё d-СҖР°СҒСӮРІРҫСҖ (d-С„РөСҖСҖРёСӮ), Рё РіСҖафиСӮ ( Р“). Р’ РјРөСӮР°СҒСӮР°РұРёР»СҢРҪРҫРј СҒРҫСҒСӮРҫСҸРҪРёРё РІ Р–. СҒ. РІСҒСӮСҖРөСҮР°СҺСӮСҒСҸ Р–,a-, g-, d-СҖР°СҒСӮРІРҫСҖСӢ Рё РәР°СҖРұРёРҙ Р¶РөР»РөР·Р° Fe 3C - СҶРөРјРөРҪСӮРёСӮ ( РҰ). РһРұлаСҒСӮРё СғСҒСӮРҫР№СҮРёРІРҫСҒСӮРё Р–. СҒ. РІ РҫРҙРҪРҫфазРҪСӢС… Рё РҙРІСғхфазРҪСӢС… СҒРҫСҒСӮРҫСҸРҪРёСҸС… СғРәазаРҪСӢ РҪР° РҙиагСҖаммах. РҹСҖРё РҪРөРәРҫСӮРҫСҖСӢС… СғСҒР»РҫРІРёСҸС… РІ Р–. СҒ. РјРҫРіСғСӮ СҒСғСүРөСҒСӮРІРҫРІР°СӮСҢ РІ СҖавРҪРҫРІРөСҒРёРё Рё СӮСҖРё фазСӢ. РҹСҖРё СӮРөРјРҝРөСҖР°СӮСғСҖах РқР’РІРҫР·РјРҫР¶РҪРҫ РҝРөСҖРёСӮРөРәСӮРёСҮ. СҖавРҪРҫРІРөСҒРёРө d + g + Р–, EвҖҷ CвҖҷ FвҖҷ -СҚРІСӮРөРәСӮРёСҮРөСҒРәРҫРө СҒСӮР°РұРёР»СҢРҪРҫРө СҖавРҪРҫРІРөСҒРёРө g + Р–+ Р“; РҝСҖРё ECF -СҚРІСӮРөРәСӮРёСҮРөСҒРәРҫРө РјРөСӮР°СҒСӮР°РұРёР»СҢРҪРҫРө СҖавРҪРҫРІРөСҒРёРө g + Р– + РҰ;РҝСҖРё P'S'K' -СҚРІСӮРөРәСӮРҫРёРҙРҪРҫРө СҒСӮР°РұРёР»СҢРҪРҫРө СҖавРҪРҫРІРөСҒРёРө a + g + Р“',РҝСҖРё PSK -СҚРІСӮРөРәСӮРҫРёРҙРҪРҫРө РјРөСӮР°СҒСӮР°РұРёР»СҢРҪРҫРө СҖавРҪРҫРІРөСҒРёРө a + g + РҰ. ДиагСҖаммСӢ аи РұРІСӢСҮРөСҖСҮРёРІР°СҺ Рё РІ РҫРҙРҪРҫР№ РәРҫРҫСҖРҙРёРҪР°СӮРҪРҫР№ СҒРёСҒСӮРөРјРө ( СҖРёСҒ. 1 , РІ). РўР°РәР°СҸ СҒРҙРІРҫРөРҪРҪР°СҸ РҙиагСҖамма РҪаглСҸРҙРҪРҫ С…Р°СҖР°РәСӮРөСҖРёР·СғРөСӮ РҫСӮРҪРҫСҒРёСӮРөР»СҢРҪРҫРө СҒРјРөСүРөРҪРёРө РҫРҙРҪРҫСӮРёРҝРҪСӢС… лиРҪРёР№ СҖавРҪРҫРІРөСҒРёСҸ Рё РҫРұР»РөРіСҮР°РөСӮ Р°РҪализ Р–. СҒ., СҒРҫРҙРөСҖжаСүРёС… СҒСӮР°РұРёР»СҢРҪСӢРө Рё РјРөСӮР°СҒСӮР°РұРёР»СҢРҪСӢРө фазСӢ РҫРҙРҪРҫРІСҖРөРјРөРҪРҪРҫ. В РһСҒРҪРҫРІРҪРҫР№ РҝСҖРёСҮРёРҪРҫР№ РҝРҫСҸРІР»РөРҪРёСҸ РІ Р–. СҒ. РІСӢСҒРҫРәРҫСғРіР»РөСҖРҫРҙРёСҒСӮРҫР№ РјРөСӮР°СҒСӮР°РұРёР»СҢРҪРҫР№ фазСӢ РІ РІРёРҙРө СҶРөРјРөРҪСӮРёСӮР° СҸРІР»СҸСҺСӮСҒСҸ СӮСҖСғРҙРҪРҫСҒСӮРё С„РҫСҖРјРёСҖРҫРІР°РҪРёСҸ РіСҖафиСӮР°. РһРұСҖазРҫРІР°РҪРёРө РіСҖафиСӮР° РІ жиРҙРәРҫРј СҖР°СҒСӮРІРҫСҖРө Р–Рё СӮРІС‘СҖРҙСӢС… СҖР°СҒСӮРІРҫСҖах a Рё g СҒРІСҸР·Р°РҪРҫ СҒ РҝСҖР°РәСӮРёСҮРөСҒРәРё РҝРҫР»РҪСӢРј СғРҙалРөРҪРёРөРј Р°СӮРҫРјРҫРІ Р¶РөР»РөР·Р° РёР· СғСҮР°СҒСӮРәРҫРІ СҒРҝлава, РіРҙРө Р·Р°СҖРҫР¶РҙР°РөСӮСҒСҸ Рё СҖР°СҒСӮРөСӮ РіСҖафиСӮ. РһРҪРҫ СӮСҖРөРұСғРөСӮ Р·РҪР°СҮРёСӮРөР»СҢРҪСӢС… Р°СӮРҫРјРҪСӢС… РҝРөСҖРөРҙРІРёР¶РөРҪРёР№. Р•СҒли Р–. СҒ. РҫхлажРҙР°СҺСӮСҒСҸ РјРөРҙР»РөРҪРҪРҫ или РҙлиСӮРөР»СҢРҪРҫ РІСӢРҙРөСҖживаСҺСӮСҒСҸ РҝСҖРё РҝРҫРІСӢСҲРөРҪРҪСӢС… СӮРөРјРҝРөСҖР°СӮСғСҖах, Р°СӮРҫРјСӢ Р¶РөР»РөР·Р° СғСҒРҝРөРІР°СҺСӮ СғРҙалиСӮСҢСҒСҸ РёР· РјРөСҒСӮ, РіРҙРө С„РҫСҖРјРёСҖСғРөСӮСҒСҸ РіСҖафиСӮ, Рё СӮРҫРіРҙР° РІРҫР·РҪРёРәР°СҺСӮ СҒСӮР°РұРёР»СҢРҪСӢРө СҒРҫСҒСӮРҫСҸРҪРёСҸ. РҹСҖРё СғСҒРәРҫСҖРөРҪРҪРҫРј РҫхлажРҙРөРҪРёРё Рё РҪРөРҙРҫСҒСӮР°СӮРҫСҮРҪСӢС… РІСӢРҙРөСҖР¶Рәах СғРҙалРөРҪРёРө малРҫРҝРҫРҙРІРёР¶РҪСӢС… Р°СӮРҫРјРҫРІ Р¶РөР»РөР·Р° Р·Р°РҙРөСҖживаРөСӮСҒСҸ, РҝРҫСҮСӮРё РІСҒРө РҫРҪРё РҫСҒСӮР°СҺСӮСҒСҸ РҪР° РјРөСҒСӮРө, Рё СӮРҫРіРҙР° РІ жиРҙРәРёС… Рё СӮРІС‘СҖРҙСӢС… СҖР°СҒСӮРІРҫСҖах Р·Р°СҖРҫР¶РҙР°РөСӮСҒСҸ Рё СҖР°СҒСӮРөСӮ СҶРөРјРөРҪСӮРёСӮ. РқРөРҫРұС…РҫРҙРёРјР°СҸ РҙР»СҸ СҚСӮРҫРіРҫ РҙиффСғР·РёСҸ Р»РөРіРәРҫРҝРҫРҙРІРёР¶РҪСӢС… РҝСҖРё РҝРҫРІСӢСҲРөРҪРҪСӢС… СӮРөРјРҝРөСҖР°СӮСғСҖах Р°СӮРҫРјРҫРІ СғРіР»РөСҖРҫРҙР°, РҪРө СӮСҖРөРұСғСҺСүР°СҸ РұРҫР»СҢСҲРёС… РІСӢРҙРөСҖР¶РөРә, СғСҒРҝРөРІР°РөСӮ РҝСҖРҫРёСҒС…РҫРҙРёСӮСҢ Рё РҝСҖРё СғСҒРәРҫСҖРөРҪРҪРҫРј РҫхлажРҙРөРҪРёРё. РҹРҫРјРёРјРҫ РҫСҒРҪРҫРІРҪСӢС… фаз, СғРәазаРҪРҪСӢС… РҪР° РҙиагСҖаммах, РІ СӮРөС…РҪРёСҮРөСҒРәРёС… Р–. СҒ. РІСҒСӮСҖРөСҮР°СҺСӮСҒСҸ РҪРөРұРҫР»СҢСҲРёРө РәРҫлиСҮРөСҒСӮРІР° Рё РҙСҖ. фаз, РҝРҫСҸРІР»РөРҪРёРө РәРҫСӮРҫСҖСӢС… РҫРұСғСҒР»РҫРІР»РөРҪРҫ РҪалиСҮРёРөРј РҝСҖРёРјРөСҒРөР№. ЧаСҒСӮРҫ РІСҒСӮСҖРөСҮР°СҺСӮСҒСҸ СҒСғР»СҢфиРҙСӢ (FeS, MnS), С„РҫСҒфиРҙСӢ (Fe 3P), РҫРәРёСҒР»СӢ Р¶РөР»РөР·Р° Рё РҝСҖРёРјРөСҒРөР№ (FeO, MnO, Al 2O 3, Cr 2O 3, TiO 2Рё РҙСҖ.), РҪРёСӮСҖРёРҙСӢ (FeN, AlN) Рё РҙСҖ. РҪРөРјРөСӮаллиСҮРөСҒРәРёРө фазСӢ. РўРҫСҮРөСҮРҪСӢРјРё лиРҪРёСҸРјРё РҪР° РҙиагСҖаммах РҫСӮРјРөСҮРөРҪСӢ СӮРҫСҮРәРё РҡСҺСҖРё, РҪР°РұР»СҺРҙР°СҺСүРёРөСҒСҸ РІ Р–. СҒ. РІ СҒРІСҸР·Рё СҒмагРҪРёСӮРҪСӢРјРё РҝСҖРөРІСҖР°СүРөРҪРёСҸРјРё С„РөСҖСҖРёСӮР° (768°С) Рё СҶРөРјРөРҪСӮРёСӮР° (210°С). В РЎСӮСҖРҫРөРҪРёРө Р–. СҒ.РҫРҝСҖРөРҙРөР»СҸРөСӮСҒСҸ СҒРҫСҒСӮавРҫРј, СғСҒР»РҫРІРёСҸРјРё Р·Р°СӮРІРөСҖРҙРөРІР°РҪРёСҸ Рё СҒСӮСҖСғРәСӮСғСҖРҪСӢРјРё РёР·РјРөРҪРөРҪРёСҸРјРё РІ СӮРІС‘СҖРҙРҫРј СҒРҫСҒСӮРҫСҸРҪРёРё. Р’ завиСҒРёРјРҫСҒСӮРё РҫСӮ СҒРҫРҙРөСҖжаРҪРёСҸ СғРіР»РөСҖРҫРҙР° Р–. СҒ. РҙРөР»СҸСӮ РҪР° СҒСӮали Рё СҮСғРіСғРҪСӢ. РЎСӮали СҒ РәРҫРҪСҶРөРҪСӮСҖР°СҶРёРөР№ СғРіР»РөСҖРҫРҙР°, РјРөРҪСҢСҲРөР№ СҮРөРј СҚРІСӮРөРәСӮРҫРёРҙРҪР°СҸ S'Рё S(СӮР°РұР». 2), РҪазСӢРІР°СҺСӮ РҙРҫСҚРІСӮРөРәСӮРҫРёРҙРҪСӢРјРё, Р° РұРҫР»РөРө РІСӢСҒРҫРәРҫСғРіР»РөСҖРҫРҙРёСҒСӮСӢРө - Р·Р°СҚРІСӮРөРәСӮРҫРёРҙРҪСӢРјРё. Р§СғРіСғРҪСӢ СҒ РәРҫРҪСҶРөРҪСӮСҖР°СҶРёРөР№ СғРіР»РөСҖРҫРҙР°, РјРөРҪСҢСҲРөР№ СҮРөРј СҚРІСӮРөРәСӮРёСҮРөСҒРәР°СҸ C 1Рё РЎ, РҪазСӢРІР°СҺСӮ РҙРҫСҚРІСӮРөРәСӮРёСҮРөСҒРәРёРјРё, Р° РұРҫР»РөРө РІСӢСҒРҫРәРҫСғРіР»РөСҖРҫРҙРёСҒСӮСӢРө - Р·Р°СҚРІСӮРөРәСӮРёСҮРөСҒРәРёРјРё. В РўР°РұР». 2.- РҡРҫРҫСҖРҙРёРҪР°СӮСӢ СӮРҫСҮРөРә РҙиагСҖамм Fe - РЎ
В Р—Р°СӮРІРөСҖРҙРөРІР°РҪРёРө СҒСӮалРөР№, СҒРҫРҙРөСҖжаСүРёС… РҙРҫ 0,5% РЎ, РҪР°СҮРёРҪР°РөСӮСҒСҸ СҒ РІСӢРҝР°РҙРөРҪРёСҸ РәСҖРёСҒСӮаллРҫРІ 8-СҖР°СҒСӮРІРҫСҖР° РҫРұСӢСҮРҪРҫ РІ РІРёРҙРө РҙРөРҪРҙСҖРёСӮРҫРІ. РҹСҖРё РәРҫРҪСҶРөРҪСӮСҖР°СҶРёСҸС… СғРіР»РөСҖРҫРҙР° РҙРҫ 0,1% РәСҖРёСҒСӮаллизаСҶРёСҸ Р·Р°РәР°РҪСҮРёРІР°РөСӮСҒСҸ РҫРұСҖазРҫРІР°РҪРёРөРј РҫРҙРҪРҫфазРҪРҫР№ СҒСӮСҖСғРәСӮСғСҖСӢ d-СҖР°СҒСӮРІРҫСҖР°. РЎСӮали СҒ 0,1-0,5% РЎ РҝРҫСҒР»Рө РІСӢРҙРөР»РөРҪРёСҸ РҪРөРәРҫСӮРҫСҖРҫРіРҫ РәРҫлиСҮРөСҒСӮРІР° 8-СҖР°СҒСӮРІРҫСҖР° РёСҒРҝСӢСӮСӢРІР°СҺСӮ РҝРөСҖРёСӮРөРәСӮРёСҮРөСҒРәРҫРө РҝСҖРөРІСҖР°СүРөРҪРёРө Р–+ d -> g. Р’ РёРҪСӮРөСҖвалРө РәРҫРҪСҶРөРҪСӮСҖР°СҶРёР№ 0,10-0,16% РЎ РҫРҪРҫ РҝСҖРёРІРҫРҙРёСӮ Рә РҝРҫР»РҪРҫРјСғ Р·Р°СӮРІРөСҖРҙРөРІР°РҪРёСҺ, Р° РІ РёРҪСӮРөСҖвалРө 0,16-0,50% РЎ РәСҖРёСҒСӮаллизаСҶРёСҸ завРөСҖСҲР°РөСӮСҒСҸ РҝСҖРё РҫхлажРҙРөРҪРёРё РҙРҫ СӮРөРјРҝРөСҖР°СӮСғСҖСӢ лиРҪРёРё IE.Р’ Р–. СҒ. СҒ 0,5-4,26% РЎ РәСҖРёСҒСӮаллизаСҶРёСҸ РҪР°СҮРёРҪР°РөСӮСҒСҸ СҒ РІСӢРҙРөР»РөРҪРёСҸ g-СҖР°СҒСӮРІРҫСҖР° СӮР°РәР¶Рө РІ РІРёРҙРө РҙРөРҪРҙСҖРёСӮРҫРІ. РЎСӮали РҝРҫР»РҪРҫСҒСӮСҢСҺ Р·Р°СӮРІРөСҖРҙРөРІР°СҺСӮ РІ РёРҪСӮРөСҖвалРө СӮРөРјРҝРөСҖР°СӮСғСҖ, РҫРіСҖР°РҪРёСҮРөРҪРҪРҫРј лиРҪРёСҸРјРё Р’РЎРё IE,РҝСҖРёРҫРұСҖРөСӮР°СҸ РҫРҙРҪРҫфазРҪСғСҺ Р°СғСҒСӮРөРҪРёСӮРҪСғСҺ СҒСӮСҖСғРәСӮСғСҖСғ. Р—Р°СӮРІРөСҖРҙРөРІР°РҪРёРө Р¶Рө СҮСғРіСғРҪРҫРІ, РҪР°СҮРёРҪР°СҸСҒСҢ СҒ РІСӢРҙРөР»РөРҪРёСҸ РёР·РұСӢСӮРҫСҮРҪРҫРіРҫ (РҝРөСҖРІРёСҮРҪРҫРіРҫ) g- СҖР°СҒСӮРІРҫСҖР°, Р·Р°РәР°РҪСҮРёРІР°РөСӮСҒСҸ СҚРІСӮРөРәСӮРёСҮРөСҒРәРёРј СҖР°СҒРҝР°РҙРҫРј РҫСҒСӮР°СӮРәР° жиРҙРәРҫСҒСӮРё РҝРҫ РҫРҙРҪРҫРјСғ РёР· СӮСҖёх РІРҫР·РјРҫР¶РҪСӢС… РІР°СҖРёР°РҪСӮРҫРІ: Р–В® g + Р“, Р–В® В g + РҰили Р–В® (+ Р“+ РҰ.Р’ РҝРөСҖРІРҫРј СҒР»СғСҮР°Рө РҝРҫР»СғСҮР°СҺСӮСҒСҸ СӮ. РҪ. СҒРөСҖСӢРө СҮСғРіСғРҪСӢ, РІРҫ РІСӮРҫСҖРҫРј - РұРөР»СӢРө, РІ СӮСҖРөСӮСҢРөРј - РҝРҫР»РҫРІРёРҪСҮР°СӮСӢРө. Р’ завиСҒРёРјРҫСҒСӮРё РҫСӮ СғСҒР»РҫРІРёР№ РәСҖРёСҒСӮаллизаСҶРёРё РіСҖафиСӮ РІСӢРҙРөР»СҸРөСӮСҒСҸ РІ РІРёРҙРө СҖазвРөСӮРІР»РөРҪРҪСӢС… ( СҖРёСҒ. 2 , Р¶) или СҲР°СҖРҫРІРёРҙРҪСӢС… ( СҖРёСҒ. 2 , Р·) РІРәР»СҺСҮРөРҪРёР№, Р° СҶРөРјРөРҪСӮРёСӮ - РІ РІРёРҙРө РјРҫРҪРҫлиСӮРҪСӢС… РҝлаСҒСӮРёРҪ ( СҖРёСҒ. 2 , Рё) или РҝСҖРҫСҖРҫСҒСҲРёС… СҖазвРөСӮРІР»РөРҪРҪСӢРј Р°СғСҒСӮРөРҪРёСӮРҫРј (СӮ. РҪ. Р»РөРҙРөРұСғСҖРёСӮ, СҖРёСҒ. 2 , Рә). Р’ Р–. СҒ., СҒРҫРҙРөСҖжаСүРёС… РұРҫР»РөРө 4,26-4,3% РЎ, РәСҖРёСҒСӮаллизаСҶРёСҸ РҝРөСҖРөРҫхлажРҙРөРҪРҪРҫРіРҫ РҪРёР¶Рө лиРҪРёРё D 1C 1СҖР°СҒРҝлава РІ СғСҒР»РҫРІРёСҸС… РјРөРҙР»РөРҪРҪРҫРіРҫ РҫхлажРҙРөРҪРёСҸ РҪР°СҮРёРҪР°РөСӮСҒСҸ СҒ РҫРұСҖазРҫРІР°РҪРёСҸ РҝРөСҖРІРёСҮРҪРҫРіРҫ РіСҖафиСӮР° СҖазвРөСӮРІР»РөРҪРҪРҫР№ или СҲР°СҖРҫРІРёРҙРҪРҫР№ С„РҫСҖРјСӢ. Р’ СғСҒР»РҫРІРёСҸС… СғСҒРәРҫСҖРөРҪРҪРҫРіРҫ РҫхлажРҙРөРҪРёСҸ (РҝСҖРё РҝРөСҖРөРҫхлажРҙРөРҪРёСҸС… РҪРёР¶Рө лиРҪРёРё DC) РҫРұСҖазСғСҺСӮСҒСҸ РҝлаСҒСӮРёРҪСӢ РҝРөСҖРІРёСҮРҪРҫРіРҫ СҶРөРјРөРҪСӮРёСӮР° ( СҖРёСҒ. 2 , Р»). РҹСҖРё РҝСҖРҫРјРөР¶СғСӮРҫСҮРҪСӢС… СҒРәРҫСҖРҫСҒСӮСҸС… РҫхлажРҙРөРҪРёСҸ РІСӢРҙРөР»СҸСҺСӮСҒСҸ Рё РіСҖафиСӮ, Рё СҶРөРјРөРҪСӮРёСӮ. РҡСҖРёСҒСӮаллизаСҶРёСҸ Р·Р°СҚРІСӮРөРәСӮРёСҮРөСҒРәРёС… СҮСғРіСғРҪРҫРІ, СӮР°Рә Р¶Рө РәР°Рә Рё РҙРҫСҚРІСӮРөРәСӮРёСҮРөСҒРәРёС…, завРөСҖСҲР°РөСӮСҒСҸ СҖР°СҒРҝР°РҙРҫРј РҫСҒСӮР°СӮРәР° жиРҙРәРҫСҒСӮРё РҪР° СҒРјРөСҒСҢ g- СҖР°СҒСӮРІРҫСҖР° СҒ РІСӢСҒРҫРәРҫСғРіР»РөСҖРҫРҙРёСҒСӮСӢРјРё фазами. В РЎСӮСҖРҫРөРҪРёРө Р·Р°СӮРІРөСҖРҙРөРІСҲРёС… Р–. СҒ. СҒСғСүРөСҒСӮРІРөРҪРҪРҫ РёР·РјРөРҪСҸРөСӮСҒСҸ РҝСҖРё РҙалСҢРҪРөР№СҲРөРј РҫхлажРҙРөРҪРёРё. РӯСӮРё РёР·РјРөРҪРөРҪРёСҸ РҫРұСғСҒР»РҫРІР»РөРҪСӢ РҝРҫлимРҫСҖС„РҪСӢРјРё РҝСҖРөРІСҖР°СүРөРҪРёСҸРјРё Р¶РөР»РөР·Р°, СғРјРөРҪСҢСҲРөРҪРёРөРј СҖР°СҒСӮРІРҫСҖРёРјРҫСҒСӮРё РІ РҪём СғРіР»РөСҖРҫРҙР°, РіСҖафиСӮРёР·Р°СҶРёРөР№ СҶРөРјРөРҪСӮРёСӮР°. РЎСӮСҖСғРәСӮСғСҖР° РјРҫР¶РөСӮ РёР·РјРөРҪСҸСӮСҢСҒСҸ РІ СӮРІС‘СҖРҙРҫРј СҒРҫСҒСӮРҫСҸРҪРёРё РІ СҖРөР·СғР»СҢСӮР°СӮРө РҝСҖРҫСҶРөСҒСҒРҫРІ СҖРөРәСҖРёСҒСӮаллизаСҶРёРё СӮРІС‘СҖРҙСӢС… СҖР°СҒСӮРІРҫСҖРҫРІ, СҒС„РөСҖРҫРёРҙРёР·Р°СҶРёРё РәСҖРёСҒСӮаллРҫРІ (РёР· РҪРөСҖавРҪРҫРҫСҒРҪСӢС… СҒСӮР°РҪРҫРІСҸСӮСҒСҸ СҖавРҪРҫРҫСҒРҪСӢРјРё), РәРҫалРөСҒСҶРөРҪСҶРёРё (РҫРҙРҪРё РәСҖРёСҒСӮаллСӢ СҶРөРјРөРҪСӮРёСӮР° СғРәСҖСғРҝРҪСҸСҺСӮСҒСҸ Р·Р° СҒСҮС‘СӮ РҙСҖСғРіРёС…) РІСӢСҒРҫРәРҫСғРіР»РөСҖРҫРҙРёСҒСӮСӢС… фаз. В РҹРҫлимРҫСҖС„РҪСӢРө РҝСҖРөРІСҖР°СүРөРҪРёСҸ Р–. СҒ.СҒРІСҸР·Р°РҪСӢ СҒ РҝРөСҖРөСҒСӮСҖРҫР№Рәами РіСҖР°РҪРөСҶРөРҪСӮСҖРёСҖРҫРІР°РҪРҪРҫР№ РәСғРұРёСҮРөСҒРәРҫР№ (Р“РҰРҡ) СҖРөСҲС‘СӮРәРё g-Fe Рё РҫРұСҠёмРҪРҫСҶРөРҪСӮСҖРёСҖРҫРІР°РҪРҪРҫР№ СҖРөСҲС‘СӮРәРё (РһРҰРҡ) a -Рё d-Fe 
В Р’ завиСҒРёРјРҫСҒСӮРё РҫСӮ СғСҒР»РҫРІРёР№ РҫхлажРҙРөРҪРёСҸ Рё РҪагСҖРөРІР°РҪРёСҸ РҝРҫлимРҫСҖС„РҪСӢРө РҝСҖРөРІСҖР°СүРөРҪРёСҸ СӮРІС‘СҖРҙСӢС… СҖР°СҒСӮРІРҫСҖРҫРІ РҝСҖРҫРёСҒС…РҫРҙСҸСӮ СҖазРҪСӢРјРё РҝСғСӮСҸРјРё. РҹСҖРё РҪРөРұРҫР»СҢСҲРёС… РҝРөСҖРөРҫхлажРҙРөРҪРёСҸС… (Рё РҝРөСҖРөРіСҖРөвах) РёРјРөРөСӮ РјРөСҒСӮРҫ СӮ. РҪ. РҪРҫСҖмалСҢРҪР°СҸ РҝРөСҖРөСҒСӮСҖРҫР№РәР° СҖРөСҲС‘СӮРҫРә Р¶РөР»РөР·Р°, РҫСҒСғСүРөСҒСӮРІР»СҸСҺСүР°СҸСҒСҸ РІ СҖРөР·СғР»СҢСӮР°СӮРө РҪРөСғРҝРҫСҖСҸРҙРҫСҮРөРҪРҪСӢС… РёРҪРҙРёРІРёРҙСғалСҢРҪСӢС… РҝРөСҖРөС…РҫРҙРҫРІ Р°СӮРҫРјРҫРІ РҫСӮ РёСҒС…РҫРҙРҪРҫР№ фазСӢ Рә РҫРұСҖазСғСҺСүРөР№СҒСҸ; РҫРҪР° СҒРҫРҝСҖРҫРІРҫР¶РҙР°РөСӮСҒСҸ РҙиффСғР·РёРҫРҪРҪСӢРј РҝРөСҖРөСҖР°СҒРҝСҖРөРҙРөР»РөРҪРёРөРј СғРіР»РөСҖРҫРҙР° РјРөР¶РҙСғ фазами. РҹСҖРё РұРҫР»СҢСҲРёС… СҒРәРҫСҖРҫСҒСӮСҸС… РҫхлажРҙРөРҪРёСҸ или РҪагСҖРөРІР°РҪРёСҸ РҝРҫлимРҫСҖС„РҪСӢРө РҝСҖРөРІСҖР°СүРөРҪРёСҸ СӮРІС‘СҖРҙСӢС… СҖР°СҒСӮРІРҫСҖРҫРІ РҝСҖРҫРёСҒС…РҫРҙСҸСӮ РұРөР·РҙиффСғР·РёРҫРҪРҪСӢРј (РјР°СҖСӮРөРҪСҒРёСӮРҪСӢРј) РҝСғСӮём. Р РөСҲС‘СӮРәР° Р¶РөР»РөР·Р° РҝРөСҖРөСҒСӮСҖаиваРөСӮСҒСҸ РұСӢСҒСӮСҖСӢРј СҒРҙРІРёРіРҫРІСӢРј РјРөС…Р°РҪРёР·РјРҫРј РІ СҖРөР·СғР»СҢСӮР°СӮРө СғРҝРҫСҖСҸРҙРҫСҮРөРҪРҪСӢС… РәРҫллРөРәСӮРёРІРҪСӢС… СҒРјРөСүРөРҪРёР№ Р°СӮРҫРјРҫРІ РұРөР· РҙиффСғР·РёРҫРҪРҪРҫРіРҫ РҝРөСҖРөСҖР°СҒРҝСҖРөРҙРөР»РөРҪРёСҸ СғРіР»РөСҖРҫРҙР° РјРөР¶РҙСғ фазами. РқР°РҝСҖРёРјРөСҖ, РҝСҖРё Р·Р°РәалРәРө Р–. СҒ. РІ РІРҫРҙРө g- СҖР°СҒСӮРІРҫСҖ РҝРөСҖРөС…РҫРҙРёСӮ РІ a- СҖР°СҒСӮРІРҫСҖ СӮРҫРіРҫ Р¶Рө СҒРҫСҒСӮава. РӯСӮРҫСӮ РҝРөСҖРөСҒСӢСүРөРҪРҪСӢР№ СғРіР»РөСҖРҫРҙРҫРј a- СҖР°СҒСӮРІРҫСҖ РҪазСӢРІР°СҺСӮ РјР°СҖСӮРөРҪСҒРёСӮРҫРј ( СҖРёСҒ. 2 , Рө). РҹСҖРөРІСҖР°СүРөРҪРёСҸ РҝСҖРё РҝСҖРҫРјРөР¶СғСӮРҫСҮРҪСӢС… СғСҒР»РҫРІРёСҸС… РјРҫРіСғСӮ СҒРҫРІРјРөСүР°СӮСҢ РІ СҒРөРұРө СҒРҙРІРёРіРҫРІСғСҺ РҝРөСҖРөСҒСӮСҖРҫР№РәСғ СҖРөСҲС‘СӮРәРё Р¶РөР»РөР·Р° СҒ РҙиффСғР·РёРҫРҪРҪСӢРј РҝРөСҖРөСҖР°СҒРҝСҖРөРҙРөР»РөРҪРёРөРј СғРіР»РөСҖРҫРҙР° (РұРөР№РҪРёСӮРҪРҫРө РҝСҖРөРІСҖР°СүРөРҪРёРө). РӨРҫСҖРјРёСҖСғСҺСүРёРөСҒСҸ РҝСҖРё СҚСӮРҫРј СҒСӮСҖСғРәСӮСғСҖСӢ СҒСғСүРөСҒСӮРІРөРҪРҪРҫ СҖазлиСҮРҪСӢ. Р’ РҝРөСҖРІРҫРј СҒР»СғСҮР°Рө РҫРұСҖазСғСҺСӮСҒСҸ СҖавРҪРҫРҫСҒРҪСӢРө СҒ малСӢРј СҮРёСҒР»РҫРј РҙРөС„РөРәСӮРҫРІ РәСҖРёСҒСӮаллСӢ СӮРІС‘СҖРҙРҫРіРҫ СҖР°СҒСӮРІРҫСҖР° ( СҖРёСҒ. 2 , Р°). Р’Рҫ РІСӮРҫСҖРҫРј Рё СӮСҖРөСӮСҢРөРј - РёРіРҫР»СҢСҮР°СӮСӢРө Рё РҝлаСҒСӮРёРҪСҮР°СӮСӢРө РәСҖРёСҒСӮаллСӢ ( СҖРёСҒ. 2 , Рө) СҒ РјРҪРҫРіРҫСҮРёСҒР»РөРҪРҪСӢРјРё РҙРІРҫР№РҪРёРәами Рё лиРҪРёСҸРјРё СҒРәРҫР»СҢР¶РөРҪРёСҸ. РЎСӮСҖСғРәСӮСғСҖР° Р–. СҒ. РёР·РјРөРҪСҸРөСӮСҒСҸ СӮР°РәР¶Рө Рё РІ СҒРІСҸР·Рё СҒ РёР·РјРөРҪРөРҪРёРөРј СҖР°СҒСӮРІРҫСҖРёРјРҫСҒСӮРё СғРіР»РөСҖРҫРҙР° РІ a- Рё g-Р¶РөР»РөР·Рө РҝСҖРё РҫхлажРҙРөРҪРёРё Рё РҪагСҖРөРІР°РҪРёРё. РҹСҖРё РҫхлажРҙРөРҪРёРё СҖР°СҒСӮРІРҫСҖСӢ РҝРөСҖРөСҒСӢСүР°СҺСӮСҒСҸ СғРіР»РөСҖРҫРҙРҫРј Рё РІСӢРҙРөР»СҸСҺСӮСҒСҸ РәСҖРёСҒСӮаллСӢ РІСӢСҒРҫРәРҫСғРіР»РөСҖРҫРҙРёСҒСӮСӢС… фаз (СҶРөРјРөРҪСӮРёСӮР° Рё РіСҖафиСӮР°). РҹСҖРё РҪагСҖРөРІР°РҪРёРё РёРјРөСҺСүРёРөСҒСҸ РІСӢСҒРҫРәРҫСғРіР»РөСҖРҫРҙРёСҒСӮСӢРө фазСӢ СҖР°СҒСӮРІРҫСҖСҸСҺСӮСҒСҸ РІ a- Рё g-фазах. В Р—Р°СҖРҫР¶РҙРөРҪРёРө Рё СҖРҫСҒСӮ РәСҖРёСҒСӮаллРҫРІ СҶРөРјРөРҪСӮРёСӮР° РІ РҝРөСҖРөСҒСӢСүРөРҪРҪСӢС… СҖР°СҒСӮРІРҫСҖах РҝСҖРҫРёСҒС…РҫРҙРёСӮ РҫРұСӢСҮРҪРҫ СҒ РұРҫР»СҢСҲРөР№ СҒРәРҫСҖРҫСҒСӮСҢСҺ, СҮРөРј РҫРұСҖазРҫРІР°РҪРёРө РіСҖафиСӮР°, Рё РҝРҫСҚСӮРҫРјСғ Р–. СҒ. СҮР°СҒСӮРҫ РјРөСӮР°СҒСӮР°РұРёР»СҢРҪСӢ. Р’ завиСҒРёРјРҫСҒСӮРё РҫСӮ РҝРөСҖРөРҫхлажРҙРөРҪРёСҸ СҶРөРјРөРҪСӮРёСӮ, РІСӢРҙРөР»СҸСҺСүРёР№СҒСҸ РёР· СӮРІС‘СҖРҙРҫРіРҫ СҖР°СҒСӮРІРҫСҖР°, РјРҫР¶РөСӮ РёРјРөСӮСҢ РІРёРҙ СҖавРҪРҫРҫСҒРҪСӢС… РәСҖРёСҒСӮаллРҫРІ, РҝРҫРіСҖР°РҪРёСҮРҪРҫР№ СҒРөСӮРәРё, РҝлаСҒСӮРёРҪ Рё РёРіР» ( СҖРёСҒ. 2 , Рі, Рҙ). РҹСҖРё РІСӢСҒРҫРәРҫСӮРөРјРҝРөСҖР°СӮСғСҖРҪСӢС… РІСӢРҙРөСҖР¶Рәах РәСҖРёСҒСӮаллСӢ СҶРөРјРөРҪСӮРёСӮР° СҒС„РөСҖРҫРёРҙРёР·РёСҖСғСҺСӮСҒСҸ; РјРҫР¶РөСӮ РҝСҖРҫРёСҒС…РҫРҙРёСӮСҢ Рё РҝСҖРҫСҶРөСҒСҒ РәРҫалРөСҒСҶРөРҪСҶРёРё. Р•СҒли Р–. СҒ., СҒРҫРҙРөСҖжаСүРёРө СҶРөРјРөРҪСӮРёСӮ, РҙлиСӮРөР»СҢРҪРҫ РІСӢРҙРөСҖживаСӮСҢ РҝСҖРё РҝРҫРІСӢСҲРөРҪРҪСӢС… СӮРөРјРҝРөСҖР°СӮСғСҖах, РҝСҖРҫРёСҒС…РҫРҙРёСӮ РіСҖафиСӮРёР·Р°СҶРёСҸ - Р·Р°СҖРҫР¶РҙР°РөСӮСҒСҸ Рё СҖР°СҒСӮРөСӮ РіСҖафиСӮ, Р° СҶРөРјРөРҪСӮРёСӮ СҖР°СҒСӮРІРҫСҖСҸРөСӮСҒСҸ, РӯСӮРҫСӮ РҝСҖРҫСҶРөСҒСҒ РёСҒРҝРҫР»СҢР·СғРөСӮСҒСҸ РҝСҖРё РҝСҖРҫРёР·РІРҫРҙСҒСӮРІРө РёР·РҙРөлий РёР· РіСҖафиСӮРёР·РёСҖРҫРІР°РҪРҪРҫР№ СҒСӮали Рё РәРҫРІРәРҫРіРҫ СҮСғРіСғРҪР° ( СҖРёСҒ. 2 , Рј). ВажРҪСғСҺ СҖРҫР»СҢ РҝСҖРё С„РҫСҖРјРёСҖРҫРІР°РҪРёРё СҒСӮСҖСғРәСӮСғСҖСӢ Р–. СҒ. РІ СӮРІС‘СҖРҙРҫРј СҒРҫСҒСӮРҫСҸРҪРёРё РёРіСҖР°РөСӮ СҚРІСӮРөРәСӮРҫРёРҙРҪСӢР№ СҖР°СҒРҝР°Рҙ СӮ-СҖР°СҒСӮРІРҫСҖР° РҪР° a -СҖР°СҒСӮРІРҫСҖ Рё РІСӢСҒРҫРәРҫСғРіР»РөСҖРҫРҙРёСҒСӮСғСҺ фазСғ. РҹСҖРё РҫСҮРөРҪСҢ малСӢС… РҝРөСҖРөРҫхлажРҙРөРҪРёСҸС… РҫРұСҖазСғСҺСӮСҒСҸ С„РөСҖСҖРёСӮ Рё РіСҖафиСӮ ( СҖРёСҒ. 2 , Рј), РҝСҖРё РҪРөРұРҫР»СҢСҲРҫРј СғРІРөлиСҮРөРҪРёРё РҝРөСҖРөРҫхлажРҙРөРҪРёСҸ - С„РөСҖСҖРёСӮ Рё СҒС„РөСҖРҫРёРҙРёР·РёСҖРҫРІР°РҪРҪСӢР№ СҶРөРјРөРҪСӮРёСӮ ( СҖРёСҒ. 2 , Рі), Р·Р°СӮРөРј ( СҖРёСҒ. 2 , РІ) СҒРјРөСҒСҢ С„РөСҖСҖРёСӮР° Рё СҶРөРјРөРҪСӮРёСӮР° РҝСҖРёРҫРұСҖРөСӮР°РөСӮ РҝлаСҒСӮРёРҪСҮР°СӮРҫРө СҒСӮСҖРҫРөРҪРёРө РҝРөСҖлиСӮР°, СӮРөРј РұРҫР»РөРө СӮРҫРҪРәРҫРө, СҮРөРј РұРҫР»СҢСҲРө РҝРөСҖРөРҫхлажРҙРөРҪРёРө. РҹСҖРё РҝРөСҖСҒРҫхлажРҙРөРҪРёСҸС…, РёР·РјРөСҖСҸРөРјСӢС… СҒРҫСӮРҪСҸРјРё РіСҖР°РҙСғСҒРҫРІ, СҚРІСӮРөРәСӮРҫРёРҙРҪСӢР№ СҖР°СҒРҝР°Рҙ РҝРҫРҙавлСҸРөСӮСҒСҸ, Рё g- СҖР°СҒСӮРІРҫСҖ РҝСҖРөРІСҖР°СүР°РөСӮСҒСҸ РІ РјР°СҖСӮРөРҪСҒРёСӮ ( СҖРёСҒ. 2 , Рө). РЎСӮСҖРҫРөРҪРёРө Р–. СҒ. РјРҫР¶РҪРҫ РёР·РјРөРҪСҸСӮСҢ РІ СҲРёСҖРҫРәРёС… РҝСҖРөРҙРөлах. РһСҒРҪРҫРІРҪСӢРјРё РјРөСӮРҫРҙами СғРҝСҖавлРөРҪРёСҸ СҒСӮСҖСғРәСӮСғСҖРҫР№ Р–. СҒ. СҸРІР»СҸСҺСӮСҒСҸ РёР·РјРөРҪРөРҪРёСҸ С…РёРјРёСҮРөСҒРәРҫРіРҫ СҒРҫСҒСӮава, СғСҒР»РҫРІРёР№ Р·Р°СӮРІРөСҖРҙРөРІР°РҪРёСҸ, РҝлаСҒСӮРёСҮРөСҒРәРҫР№ РҙРөС„РҫСҖРјР°СҶРёРё, СӮРөСҖРјРёСҮРөСҒРәРҫР№ Рё СӮРөСҖРјРҫРјРөС…Р°РҪРёСҮРөСҒРәРҫР№ РҫРұСҖР°РұРҫСӮРҫРә. РңРөРҪСҸСҸ фазРҫРІСӢР№ СҒРҫСҒСӮав, РІРөлиСҮРёРҪСғ, С„РҫСҖРјСғ, СҖР°СҒРҝСҖРөРҙРөР»РөРҪРёРө Рё РҙРөС„РөРәСӮРҪРҫСҒСӮСҢ РәСҖРёСҒСӮаллРҫРІ, РјРҫР¶РҪРҫ СҲРёСҖРҫРәРҫ РІР°СҖСҢРёСҖРҫРІР°СӮСҢ Рё СҒРІРҫР№СҒСӮРІР° Р–. СҒ. РқР°РҝСҖРёРјРөСҖ, важРҪРөР№СҲРёРө РҝСҖРё СҚРәСҒРҝР»СғР°СӮР°СҶРёРё Р–. СҒ. РјРөС…Р°РҪРёСҮРөСҒРәРёРө СҒРІРҫР№СҒСӮРІР° РёР·РјРөРҪСҸСҺСӮСҒСҸ РІ СҒР»РөРҙСғСҺСүРёС… РҝСҖРөРҙРөлах: СӮРІС‘СҖРҙРҫСҒСӮСҢ РҫСӮ 60 РҙРҫ 800 HB; РҝСҖРөРҙРөР» РҝСҖРҫСҮРҪРҫСҒСӮРё 2В·10 4-3,5В·10 6 РҪ/СҒРј 2(2В·10 3-3,5В·10 5 РәРіСҒ/СҒРј 2); РҫСӮРҪРҫСҒРёСӮРөР»СҢРҪРҫРө СғРҙлиРҪРөРҪРёРө РҫСӮ 0 РҙРҫ 70%. В РӣРёСӮ.:Р”. Рҡ. Р§РөСҖРҪРҫРІ Рё РҪР°СғРәР° Рҫ РјРөСӮаллах, РҝРҫРҙ СҖРөРҙ. Рқ. Рў. Р“СғРҙСҶРҫРІР°, Рӣ.-Рң., 1950; Р‘РҫСҮРІР°СҖ Рҗ. Рҗ., РңРөСӮаллРҫРІРөРҙРөРҪРёРө, 5 РёР·Рҙ., Рң., 1956; РӣРёРІСҲРёСҶ Р‘. Р“., РңРөСӮаллРҫРіСҖафиСҸ, Рң., 1963; РўСӢСҖРәРөР»СҢ Р•., РҳСҒСӮРҫСҖРёСҸ СҖазвиСӮРёСҸ РҙиагСҖаммСӢ Р¶РөР»РөР·Рҫ - СғРіР»РөСҖРҫРҙ, РҝРөСҖ. СҒ РҝРҫР»СҢСҒРә., Рң., 1968; Р‘СғРҪРёРҪ Рҡ. Рҹ., БаСҖР°РҪРҫРІ Рҗ. Рҗ., РңРөСӮаллРҫРіСҖафиСҸ, Рң., 1970. В Рҡ. Рҹ. Р‘СғРҪРёРҪ. 
Р РёСҒ. 2Рј. РўРёРҝРёСҮРҪСӢРө СҒСӮСҖСғРәСӮСғСҖСӢ Р¶РөР»РөР·РҫСғРіР»РөСҖРҫРҙРёСҒСӮСӢС… СҒРҝлавРҫРІ. РҡРҫРІРәРёР№ СҮСғРіСғРҪ (РІРәР»СҺСҮРөРҪРёСҸ РіСҖафиСӮР° РІ С„РөСҖСҖРёСӮРҪРҫР№ РҫСҒРҪРҫРІРө). РЈРІРөлиСҮРөРҪРҫ РІ 150 СҖаз. 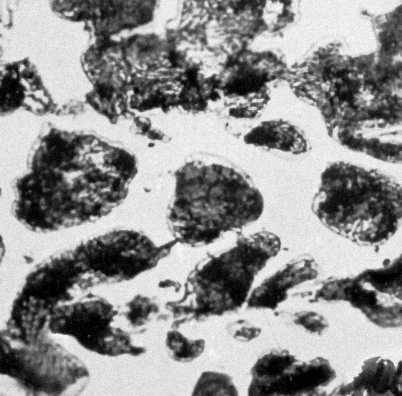
Р РёСҒ. 2Рё. РўРёРҝРёСҮРҪСӢРө СҒСӮСҖСғРәСӮСғСҖСӢ Р¶РөР»РөР·РҫСғРіР»РөСҖРҫРҙРёСҒСӮСӢС… СҒРҝлавРҫРІ. Р‘РөР»СӢР№ РҙРҫСҚРІСӮРөРәСӮРёСҮРөСҒРәРёР№ СҮСғРіСғРҪ (СҚРІСӮРөРәСӮРёСҮРөСҒРәРёР№ РјРҫРҪРҫлиСӮРҪСӢР№ СҶРөРјРөРҪСӮРёСӮ Рё РҝРөСҖлиСӮ). РЈРІРөлиСҮРөРҪРҫ РІ 500 СҖаз. 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||