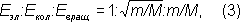|
|
Популярные авторы:: БСЭ :: Борхес Хорхе Луис :: Горький Максим :: Херберт Фрэнк :: Раззаков Федор :: Чехов Антон Павлович :: Грин Александр :: Толстой Лев Николаевич :: Азимов Айзек :: Лесков Николай Семёнович Популярные книги:: Дюна (Книги 1-3) :: The Boarding House :: Преодоление :: Три цвета времени :: Упражнения по стилистике русского языка :: Талисман из Рэдволла :: Рассказы, очерки, фельетоны :: Школа карточных фокусов :: Закрой рот, джинн – кишки простудишь… :: Андропов. 7 тайн генсека с Лубянки |
Большая Советская Энциклопедия (МО)ModernLib.Net / Энциклопедии / БСЭ / Большая Советская Энциклопедия (МО) - Чтение (стр. 24)
Молекулярное течение Молекуля'рное тече'ние,течение разреженного газа (молекул, атомов, ионов или электронов), при котором свойства потока существенно зависят от беспорядочного движения молекул, в отличие от течений, где газ рассматривается как сплошная среда. М. т. имеет место при полёте тел в верхних слоях атмосферы, в вакуумных системах и т. д. При М. т. молекулы (или другие частицы) газа участвуют, с одной стороны, в поступательном движении всего газа в целом, а с другой - двигаются хаотически и независимо друг от друга. Причём в любом рассматриваемом объёме молекулы газа могут иметь самые различные скорости. Поэтому основой теоретического рассмотрения М. т. является кинетическая теория газов.Макроскопические свойства невязкого, сжимаемого, изоэнтропического течения удовлетворительно описываются простейшей моделью молекул в виде упругих гладких шаров, которые подчиняются максвелловскому закону распределения скоростей (см. Максвелла распределение ) .Для описания вязкого, неизоэнтропического М. т. необходимо пользоваться более сложной моделью молекул и функцией распределения, которая несколько отличается от функции распределения Максвелла. М. т. исследуются в аэродинамике разреженных газов.
Лит.:Паттерсон Г. Н., Молекулярное течение газов, пер. с англ., М., 1960; Чепмен С., Каулинг Т., Математическая теория неоднородных газов, пер. с англ., М., 1960; Аэродинамика разреженных газов. Сб., под ред. С. В. Валландера, Л., 1963; Коган М. Н., Динамика разреженного газа, М., 1967. Л. В. Козлов. Молекулярной биологии институт Молекуля'рной биоло'гии институ'тАН СССР, головное научно-исследовательское учреждение в области молекулярной биологии.Организован в 1957 (до 1965 - институт радиационной и физико-химической биологии). Основатель и директор института - В. А. Энгельгардт.Основные направления научно-исследовательских работ: передача и реализация наследственной информации, молекулярные механизмы биосинтеза белка, химические и физические основы действия ферментов, связь структуры нуклеиновых кислот и белков с их функциями в клетке, макромолекулярная организация хромосом, разработка физических методов исследования макромолекул. В М. б. и. расшифрована первичная структура двух транспортных рибонуклеиновых кислот (т-РНК); экспериментально обоснована и сформулирована теория регуляции функционирования генома у высших организмов; впервые в СССР определена последовательность аминокислот в крупной молекуле белка-фермента - аспартатаминотрансферазы (совместно с институтом биоорганической химии им. М. М. Шемякина АН СССР); предложены новые подходы к изучению строения активных центров ферментов (ингибиторный анализ) и функциональных участков РНК (метод «разрезанных молекул»); разработаны новые методы структурных исследований белков и нуклеиновых кислот. К началу 1973 в М. б. и. было 13 лабораторий. Совместно с Советом по проблемам молекулярной биологии АН СССР институт организует международные совещания и симпозиумы. Труды сотрудников М. б. и. публикуются в журналах: «Молекулярная биология» (с 1967), «Биохимия» (с 1936), «Цитология» (с 1959), «Доклады АН СССР» (с 1933), «Биофизика» (с 1956), «Biochimica et Biophysica Acta» (N. Y. - Amst., с 1947), «FEBS Letters» (Amst., с 1968), «European Journal of Biochemistry» (В., с 1967), в сборниках и в виде монографий. Лит.:Институт молекулярной биологии, М., 1971. М. Я. Тимофеева. «Молекулярные болезни» «Молекуля'рные боле'зни»,врождённые ошибки метаболизма, заболевания, обусловленные наследственными нарушениями обмена веществ. Термин «М. б.» предложен американским химиком Л. Полингом.В начале 20 в. английский врач Л. Э. Гаррод, изучая ряд наследственных заболеваний,предположил, что они возникают в результате пониженной активности или полного отсутствия фермента, контролирующего определённый этап обмена веществ. Так, появление гомогентизиновой кислоты в моче больных алькаптонурией обусловлено отсутствием окисляющего её фермента (впоследствии выяснилось, что в этом случае образуется неактивная форма фермента); альбинизм вызван блокадой образования пигментов меланинов вследствие недостаточности одного из необходимых ферментов - тирозиназы и т. д. Идеи Гаррода получили всеобщее признание и конкретную химическую интерпретацию спустя несколько десятилетий. Решающими для понимания механизмов возникновения «М. б.» оказались исследования изменений биосинтеза у микроорганизмов, возникающих при замене нормального гена мутантным. Каждый нормальный ген определяет (кодирует) синтез, как правило, строго определённого фермента, т. е. нормального белка (см. Белки, Генетический код) .Изучение биохимических мутантов (работы главным образом американских генетиков Дж. Бидла и Э. Тейтема,1941) показало, что мутация гена приводит к отсутствию фермента или изменению его активности, т. е. белок либо не синтезируется вообще, либо синтезируется с измененной первичной структурой (иной последовательностью аминокислот в полипептидной цепи). Изменение первичной структуры белка (ферментного, структурного, плазмы крови), по-видимому, не влияет на его свойства («молчащие» мутации). Однако в ряде случаев (например, при изменении активного центра фермента) происходит изменение свойств, а следовательно, и функций белка. Т. о., все «М. б.» связаны либо с утратой какого-либо нормального белка, либо с изменением его ферментативных или физико-химических свойств. Поскольку каждый фермент контролирует определённую реакцию обмена веществ, его отсутствие или неспособность осуществлять свою функцию приводят к остановке нормального пути метаболизма на стадии биосинтеза вещества, являющегося субстратом этого фермента. Заболевание развивается в результате недостатка в организме конечного продукта, синтез которого блокирован, либо в результате накопления предшественника блокированной реакции, избыток которого нарушает обменные процессы. «М. б.» включают расстройства обмена аминокислот (аминоацидурии), углеводов (гликозурии), липидов (липидозы и лейкодистрофии), пуринов, пиримидинов. Всего известно свыше 1000 «М. б.». Частота каждой из «М. б.» относительно невелика: одна из самых распространённых «М. б.» - фенилкетонурия - встречается со средней частотой 1:10 000. Некоторые из наследственных нарушений обмена не влекут за собой клинические последствий (например, неспособность ощущать вкус или запах определённых веществ), другие же протекают очень тяжело. Ряд «М. б.» проявляется лишь при воздействии провоцирующих факторов внешней среды. При своевременном диагнозе некоторые «М. б.» поддаются эффективному предупреждению и лечению. Поскольку эффект мутантного гена осуществляется преимущественно в форме изменения строго определённого биосинтеза, установление наследственного характера болезни (с помощью различных методов биохимического анализа) открывает возможность воздействия на всю цепь реакций, ведущих к биохимическим и физиологическим аномалиям. Заместительная терапия применяется при гормональных заболеваниях (сахарный диабет лечат инсулином, наследственные формы гипотиреоза - гормоном щитовидной железы). Для лечения ряда «М. б.» эффективно применение ограничительных диет, из которых изъято вещество (аминокислота, углевод), накапливающееся в организме. Предупреждение «М. б.» осуществляется путём медико-генетического консультирования семей, в которых выявлены носители «М. б.». Для ряда «М. б.» разработаны методы ранней (в т. ч. внутриутробной) диагностики. Некоторые«М. б.», например т. н. эритроцитопатии, широко распространились в Африке и странах Средиземноморья, т. к. превращают аномальный эритроцит в среду, неблагоприятную для развития малярийного плазмодия (см. Гемоглобинопатии, Малярия) .См. также Генетика медицинская, Генетика человека, Медико-генетическая консультация.
Лит.:Цукеркандль Э., Полинг Л., Молекулярные болезни, эволюция и генная разнородность, в сборнике: Горизонты биохимии, пер. с англ., М., 1964; Эфроимсон В. П., Введение в медицинскую генетику, 2 изд., М., 1968; «Журнал Всесоюзного химического общества им. Д. И. Менделеева», 1970, т. 15, № 6 (посвящен биохимии наследственных болезней человека); Проблемы медицинской генетики, М., 1970; Gaгrod А. Е., Inborn errors of metabolism, L., 1963; The metabolic basis of inherited disease 2 ed., N. Y. - [a. o.], 1966. К. Д. Краснопольская. Молекулярные и атомные пучки Молекуля'рные и а'томные пучки',направленные потоки молекул или атомов, движущихся в вакууме практически без столкновений друг с другом и с молекулами остаточных газов. М. и а. п. позволяют изучать свойства отдельных частиц, пренебрегая эффектами, обусловленными столкновениями, кроме тех случаев, когда сами столкновения являются объектом исследований. Первый эксперимент с атомным пучком был осуществлен в 1911 французским учёным Л. Дюнуайе, который продемонстрировал прямолинейный пролёт в вакууме атомов Na. В дальнейшем эти эксперименты были продолжены О. Штерном с сотрудниками в Гамбурге (1929), которые использовали М. и а. п. для измерения скорости молекул и эффективных сечений их соударений друг с другом, а также для исследования явлений, обусловленных электронными спинами и магнитными моментами атомных ядер (см. Ядро атомное ) .В 1937 И. Раби использовал М. и а. п. в изобретённом им резонансном методе, который вначале применялся для измерения магнитных моментов ядер (1937-40), а в дальнейшем стал основным методом радиоспектроскопии,позволившим измерить с большой точностью фундаментальные характеристики молекул, атомов и атомных ядер (Н. Рамзей и др.). Источник, в котором формируются М. и а. п., представляет собой камеру, соединённую с высоковакуумным объёмом при помощи отверстия в тонкой стенке или узкого капилляра в толстой стенке. Исследуемые молекулы или атомы вводятся в камеру источника в виде газа или пара при давлении несколько мм рт. ст.Для формирования М. и а. п. давление газа в источнике должно быть достаточно малым, чтобы средняя длина lсвободного пробега частиц внутри источника была равна или несколько больше диаметра соединительного отверстия. В этом случае частицы вылетают из источника независимо друг от друга. Для капилляра длина lдолжна быть соизмерима также с длиной капилляра. Чрезмерное увеличение lза счёт уменьшения давления в источнике, не улучшая существенно свойств М. и а. п., уменьшает их интенсивность. Для увеличения интенсивности пучков применяют источники с несколькими отверстиями или капиллярами, расстояние между которыми должно быть несколько больше их диаметра. Соударения с частицами остаточного газа разрушают М. и а. п. тем быстрее, чем хуже вакуум. Длина М. и а. п. в идеальном вакууме была бы чрезвычайно велика, т. к. возможны были бы только соударения «догона». Молекулярное взаимодействие.Метод М. и а. п. даёт возможность детально изучать акт столкновения между двумя частицами, в отличие от химических и газодинамических методов, в которых из-за множественных столкновений частиц друг с другом наблюдаются лишь усреднённые эффекты. В некоторых из этих экспериментов измеряются эффективные сечения упругих и неупругих соударений частиц, движущихся под разными углами и с разными скоростями. В др. экспериментах наблюдаются химические реакции между частицами и изучается угловое и энергетическое распределение продуктов реакции (Лестер, 1971; Дж. Росс, 1966; Р. Дж. Гордон и др., 1971). Типичный эксперимент второго рода показан на рис. 1 . Атомы водорода вылетают из источника в вакуумную камеру, где они сталкиваются с двухатомными молекулами щелочного металла, например К 2. Угловое распределение продуктов реакции измеряется с помощью детекторов с поверхностной ионизацией (горячие нити Pt и W). Т. к. вольфрамовый детектор одинаково чувствителен к частицам K 2и KOH, а платиновый - менее чувствителен к KOH, то, комбинируя оба детектора, можно различать эти молекулы. Иногда М. и а. п. предварительно поляризуют или, наоборот, измеряют появляющуюся поляризацию. В некоторых экспериментах исследуется возбуждение колебательных уровней энергии у продуктов реакции. Резонансные эксперименты (метод Раби).Частицы, вылетая из источника в вакуум (13,3 мн/м 2или 10 -7 мм рт. ст.) ,пролетают через неоднородное магнитное поле, создаваемое магнитом А( рис. 2 ). Неоднородное поле Аискривляет их траектории, что обусловлено взаимодействием их магнитных моментов с неоднородным магнитным полем. Далее частицы пролетают через коллиматор и попадают в область детектора, где происходит компенсация искривления траектории в неоднородном магнитном поле, создаваемом магнитом В. Конфигурация поля Вв точности противоположна конфигурации поля А. Для индентификации молекул их ионизируют (электронным ударом) и пропускают через масс-спектрометр,после чего они регистрируются электронным умножителем,соединённым с фазочувствительным детектором. Плавно изменяя частоту n колебаний электромагнитного поля в зазоре магнита С, создающего однородное магнитное поле, измеряют интенсивность пучка, регистрируемого детектором. Если частота n удовлетворяет боровскому условию: n = ( E 2- E 1)/h, (1) где h - Планка постоянная , то молекулы под действием электромагнитного поля, возбуждаемого в резонаторе Р, могут переходить из состояния с энергией E 1в состояние с энергией E 2и обратно. Если по магнитным свойствам состояние E 1отличается от состояния E 2, то поле Впосле перехода молекулы обычно компенсирует отклонение, вызванное полем А, не для всех молекул пучка; часть молекул, испытавшая переход E 1® E 2, движется по траектории, показанной пунктиром ( рис. 2 ). При выполнении условия (1) интенсивность, регистрируемая детектором, имеет минимум. График зависимости интенсивности от частоты представляет собой радиочастотный спектр частиц. Зная резонансную частоту из условия (1), можно определить уровни энергии молекул (см. Магнитный резонанс ) . Метод параэлектрического резонанса аналогичен методу магнитного резонанса за исключением того, что изменения траектории обусловлены взаимодействием электрических моментов молекул с неоднородными электрическими полями, а квантовые переходы между ними вызваны колебаниями электрического поля в резонаторе. Интенсивность пучка может быть увеличена за счёт использования 4-полюсных или 6-полюсных электродов, создающих пространственную фокусировку пучка. Применяется также сочетание обоих методов, например однородное постоянное электрическое поле используют в экспериментах с магнитным резонансом, а однородное магнитное поле в опытах с параэлектрическим резонансом (К. Мак-Адан, Н. Рамзей и др., 1972). Эксперименты с магнитным и параэлектрическим резонансами в М. и а. п. дали большое количество информации о строении молекул, атомов и атомных ядер. Этим методом были измерены спины ядер, магнитные и электрические квадрупольные моменты стабильных и радиоактивных ядер. В частности, был обнаружен электрический квадрупольный момент дейтрона, что впервые указало на существование тензорных сил между элементарными частицами. Была измерена с высокой точностью тонкая структура атомных спектров, в результате чего в экспериментах с атомарным водородом был открыт Лэмбовский сдвиг, послуживший источником серии революционных теоретических открытий в квантовой электродинамике.Измерения сверхтонкой структуры спектров дали первые указания на аномальность магнитного момента электрона, которая впоследствии была измерена непосредственно. В экспериментах с М. и а. п. были осуществлены два независимых измерения постоянной тонкой структуры и получено пока единственное доказательство существования у ядер электрических октупольных моментов. Резонансные эксперименты с М. и а. п. позволили измерить вращательные магнитные моменты и электрические дипольные моменты молекул, энергию взаимодействия ядерных магнитных моментов с вращательными магнитными моментами молекул, зависимость электрических и магнитных свойств от ориентации молекул; определить квадрупольные моменты молекул, энергию межъядерных магнитных взаимодействий в молекулах и т. д. Частота колебаний, соответствующая линиям сверхтонкой структуры магнитного резонанса в М. и а. п., является основой для определения секунды в пассивных стандартах частоты (см. Квантовые стандарты частоты, Квантовые часы) . Возможность пространственной фокусировки М. и а. п., содержащих частицы в определённых энергетических состояниях при помощи неоднородных электрических или магнитных полей, позволила использовать М. и а. п. для накопления частиц в состояниях с более высокой энергией (т. е. для создания инверсии населённостей ) ,что необходимо для осуществления мазера.Первый мазер был осуществлен на пучке молекул аммиака (см. Молекулярный генератор ) .Мазер на пучке атомов водорода широко использовался как для исследования атома водорода, так и для создания активного квантового стандарта частоты. Лит.:Смит К. Ф., Молекулярные пучки, пер. с англ., М., 1959; Рамзей Н., Молекулярные пучки, пер. с англ., М., 1960; Kusch P., Huges V. W., Atomic and molecular beam spectroscopy, в кн.: Handbuch der Physik, Hrsg. von S. Flьgge, Bd 37, Tl 1, B., [u. a.], 1959; Zorn J. C., English T. C., Methods of experimental physics, v. 3, N. Y., 1973. Н. Ф. Рамзей(США). 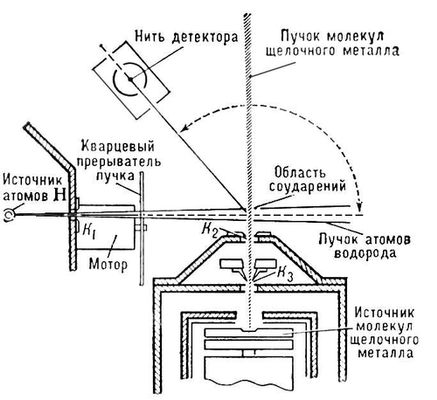
Рис. 1. Схема опыта для изучения химических реакций, происходящих при пересечении пучка атомов водорода с пучком двухатомных молекул щелочного металла. K 1, K 2, K 3- коллимирующие щели. 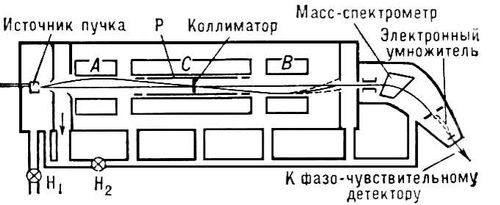
Рис. 2. Схема эксперимента по наблюдению магнитного резонанса в молекулярном пучке. Пролёт частицы через прибор определяется по искривлению её траектории; отклонения увеличены относительно типичных размеров прибора (длина прибора 3 м, максимальное поперечное сечение 0,01 см). Р - резонатор, в котором возбуждается электромагнитное поле резонансной частоты; H 1- форвакуумный насос, H 2- высоковакуумный насос; А, В и С - электромагниты. Молекулярные кристаллы Молекуля'рные криста'ллы,кристаллы, образованные из молекул, связанных друг с другом слабыми ван-дер-ваальсовыми силами (см. Межмолекулярное взаимодействие ) или водородной связью.Внутри молекул между атомами действует более прочная ковалентная связь.Фазовые превращения М. к. - плавление, возгонка, полиморфные переходы (см. Полиморфизм ) -происходят, как правило, без разрушения отдельных молекул. Большинство М. к. - кристаллы органических соединений, типичный М. к. - нафталин.М. к. образуют также некоторые простые вещества (H 2, галогены,N 2, O 2, S 8), бинарные соединения типа H 2O, CO 2, N 2O 4, металлоорганические соединения и некоторые комплексные соединения.К М. к. относятся и кристаллы полимеров,а также кристаллы белков, нуклеиновых кислот.Особым случаем М. к. являются кристаллы отвердевших инертных газов, в которых ван-дер-ваальсовы силы связывают между собой не молекулы, а атомы. Для типичных М. к. характерны низкие температуры плавления, большие коэффициенты теплового расширения, высокая сжимаемость, малая твёрдость. В обычных условиях большинство М. к. - диэлектрики.Некоторые М. к., например органические красители, - полупроводники.
Лит.:Китайгородский А. И., Молекулярные кристаллы, М., 1971; Бокий Г. Б., Кристаллохимия, М., 1971. П. М. Зоркий. Молекулярные сита Молекуля'рные си'та,сорбенты, избирательно поглощающие из окружающей среды вещества, молекулы которых не превышают определённых размеров. Такие сорбенты как бы отсеивают крупные молекулы от мелких. Различают минеральные (неорганические) и органические М. с. Неорганические М. с. имеют жёсткую кристаллическую структуру, в которой находятся полости, соединённые между собой узкими каналами «порами» или «окнами». Малые размеры «окон» препятствуют диффузии крупных молекул во внутренние полости сорбента. Некоторые алюмосиликаты - природные и синтетические цеолиты-характерные представители М. с. этого типа. Органические М. с. - гелевидные сорбенты, получаемые на основе высокомолекулярных соединений. Структура таких сорбентов представляет собой пространственную сетку из цепочечных макромолекул, «сшитых» в отдельных точках химическими связями. Из гелевидных М. с. промышленного производства наиболее распространены различные типы сефадекса - сорбента на основе декстрана (высокомолекулярного полисахарида). М. с., содержащие ионогенные (диссоциирующие на ионы) группы и способные к ионному обмену,называют ионитовыми ситами.В отличие от обычных ионитов,они избирательно поглощают из раствора лишь достаточно малые ионы, исключая из ионообменного процесса крупные ионы, диффузия которых сквозь структурную сетку сорбента затруднена. М. с. выпускают в виде порошка, зёрен неправильной формы, сферических гранул. Их используют для очистки веществ от нежелательных примесей, фракционирования синтетических полимеров, хроматографического разделения белков, углеводов, гормонов, антибиотиков и пр. Лит.:Детерман Г., Гель-хроматография, пер. с нем., М., 1970. Л. А. Шиц. Молекулярные спектры Молекуля'рные спе'ктры,оптические спектры испускания и поглощения, а также комбинационного рассеяния света,принадлежащие свободным или слабо связанным между собой молекулам.М. с. имеют сложную структуру. Типичные М. с. - полосатые, они наблюдаются в испускании и поглощении и в комбинационном рассеянии в виде совокупности более или менее узких полос в ультрафиолетовой, видимой и близкой инфракрасной областях, распадающихся при достаточной разрешающей силе применяемых спектральных приборов на совокупность тесно расположенных линий. Конкретная структура М. с. различна для различных молекул и, вообще говоря, усложняется с увеличением числа атомов в молекуле. Для весьма сложных молекул видимые и ультрафиолетовые спектры состоят из немногих широких сплошных полос; спектры таких молекул сходны между собой. М. с. возникают при квантовых переходах между уровнями энергииE‘ и E‘’ молекул согласно соотношению hn = E‘ - E‘’, (1) где hn - энергия испускаемого поглощаемого фотона частоты n ( h- Планка постоянная ) .При комбинационном рассеянии hn равно разности энергий падающего и рассеянного фотонов. М. с. гораздо сложнее линейчатых атомных спектров, что определяется большей сложностью внутренних движений в молекуле, чем в атомах. Наряду с движением электронов относительно двух или более ядер в молекулах происходят колебательное движение ядер (вместе с окружающими их внутренними электронами) около положений равновесия и вращательное движение молекулы как целого. Этим трём видам движений - электронному, колебательному и вращательному - соответствуют три типа уровней энергии и три типа спектров. Согласно квантовой механике, энергия всех видов движения в молекуле может принимать лишь определённые значения, т. е. она квантуется. Полная энергия молекулы Eприближённо может быть представлена в виде суммы квантованных значений энергий трёх видов её движения: E= E эл+ E кол+ E вращ. (2) По порядку величин
где m- масса электрона, а величина Мимеет порядок массы ядер атомов в молекуле, т. е. m/М~ 10 -3-10 -5, следовательно: E эл>> E кол>> E вращ. (4) Обычно E элпорядка нескольких эв(несколько сотен кдж/моль) , E кол~ 10 -2-10 -1 эв, E вращ~ 10 -5-10 -3 эв. В соответствии с (4) система уровней энергии молекулы характеризуется совокупностью далеко отстоящих друг от друга электронных уровней (различные значения E элпри E кол= E вращ= 0), значительно ближе друг к другу расположенных колебательных уровней (различные значения E колпри заданном E ли E вращ= 0) и ещё более близко расположенных вращательных уровней (различные значения E вращпри заданных E эли E кол). На рис. 1 приведена схема уровней двухатомной молекулы; для многоатомных молекул система уровней ещё более усложняется. Электронные уровни энергии ( E элв (2) и на схеме рис. 1 соответствуют равновесным конфигурациям молекулы (в случае двухатомной молекулы характеризуемым равновесным значением r 0межъядерного расстояния r, см. рис. 1 в ст. Молекула ) .Каждому электронному состоянию соответствуют определённая равновесная конфигурация и определённое значение E эл; наименьшее значение соответствует основному уровню энергии. Набор электронных состояний молекулы определяется свойствами её электронной оболочки. В принципе значения E элможно рассчитать методами квантовой химии,однако данная задача может быть решена только с помощью приближённых методов и для сравнительно простых молекул. Важнейшую информацию об электронных уровнях молекулы (расположение электронных уровней энергии и их характеристики), определяемую её химическим строением, получают, изучая её М. с. Весьма важная характеристика заданного электронного уровня энергии - значение квантового числаS,характеризующего абсолютную величину полного спинового момента всех электронов молекулы. Химически устойчивые молекулы имеют, как правило, чётное число электронов, и для них S= 0, 1, 2... (для основного электронного уровня типично значение S= 0, а для возбуждённых - S= 0 и S= 1). Уровни с S= 0 называются синглетными, с S= 1 - триплетными (т. к. взаимодействие в молекуле приводит к их расщеплению на c = 2 S+ 1 = 3 подуровня; см. Мультиплетность ) . Радикалы свободныеимеют, как правило, нечётное число электронов, для них S= 1/ 2, 3/ 2, ... и типично как для основного, так и для возбуждённых уровней значение S= 1/ 2(дублетные уровни, расщепляющиеся на c = 2 подуровня). Для молекул, равновесная конфигурация которых обладает симметрией, электронные уровни можно дополнительно классифицировать. В случае двухатомных и линейных трёхатомных молекул, имеющих ось симметрии (бесконечного порядка), проходящую через ядра всех атомов (см. рис. 2 , б) ,электронные уровни характеризуются значениями квантового числа l, определяющего абсолютную величину проекции полного орбитального момента всех электронов на ось молекулы. Уровни с l = 0, 1, 2, ... обозначаются соответственно S, П, D..., а величина c указывается индексом слева вверху (например, 3S, 2p, ...). Для молекул, обладающих центром симметрии, например CO 2и C 6H 6(см. рис. 2 , б, в) ,все электронные уровни делятся на чётные и нечётные, обозначаемые индексами gи u(в зависимости от того, сохраняет ли волновая функция знак при обращении в центре симметрии или меняет его). Колебательные уровни энергии (значения Е кол) можно найти квантованием колебательного движения, которое приближённо считают гармоническим. В простейшем случае двухатомной молекулы (одна колебательная степень свободы, соответствующая изменению межъядерного расстояния r) её рассматривают как гармонический осциллятор;его квантование даёт равноотстоящие уровни энергии: E кол= hn e(u + 1/2), (5) где n e- основная частота гармонических колебаний молекулы, u - колебательное квантовое число, принимающее значения 0, 1, 2, ... На рис. 1 показаны колебательные уровни для двух электронных состояний. Для каждого электронного состояния многоатомной молекулы, состоящей из Nатомов ( N³ 3) и имеющей fколебательных степеней свободы ( f= 3 N- 5 и f= 3 N- 6 для линейных и нелинейных молекул соответственно), получается fт. н. нормальных колебаний с частотами n i( i= 1, 2, 3, ..., f) и сложная система колебательных уровней: 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94 |
|||||||