 |
|
Популярные авторы:: БСЭ :: Борхес Хорхе Луис :: Горький Максим :: Азимов Айзек :: Херберт Фрэнк :: Чехов Антон Павлович :: Раззаков Федор :: Толстой Лев Николаевич :: Грин Александр :: Астафьев Виктор Петрович Популярные книги:: Дюна (Книги 1-3) :: The Boarding House :: Три цвета времени :: Упражнения по стилистике русского языка :: Преодоление :: Талисман из Рэдволла :: Плацдарм :: Закрой рот, джинн – кишки простудишь… :: Авантюристка :: Андропов. 7 тайн генсека с Лубянки |
Большая Советская Энциклопедия (МЫ)ModernLib.Net / Энциклопедии / БСЭ / Большая Советская Энциклопедия (МЫ) - Чтение (стр. 4)
Функциональные особенности гладких мышц. Гладкие М. внутренних органов по характеру иннервации, возбуждения и сокращения существенно отличаются от скелетных М. Волны возбуждения и сокращения протекают в гладких М. в очень замедленном темпе. Развитие состояния «неутомляемого» тонуса гладких М. связано, как и в тонических скелетных волокнах, с замедленностью сократительных волн, сливающихся друг с другом даже при редких ритмических раздражениях. Для гладких М. характерна также способность к автоматизму , т. е. к деятельности, не связанной с поступлением в М. нервных импульсов из центральной нервной системы. Установлено, что способностью к ритмическому самопроизвольному возбуждению и сокращению обладают не только нервные клетки, имеющиеся в гладких М., но и сами гладкомышечные клетки. Своеобразие сократительной функции гладких М. позвоночных животных определяется не только особенностями их иннервации и гистологического строения, но и спецификой их химического состава: более низким содержанием контрактильных белков (актомиозина), макроэргических соединений, в частности АТФ, низкой АТФ-азной активностью миозина, наличием в них водорастворимой модификации актомиозина - тоноактомиозина и т. д. Существенное значение для организма имеет способность гладких мышц изменять длину без повышения напряжения (наполнение полых органов, например мочевого пузыря, желудка и др.). И. И. Иванов. Скелетные мышцы человека,различные по форме, величине, положению, составляют свыше 40% массы его тела. При сокращении происходит укорочение М., которое может достигать 60% их длины; чем длиннее М. (самая длинная М. тела портняжная достигает 50 см), тем больше размах движении. Сокращение куполообразной М. (например, диафрагмы) обусловливает ее уплощение, сокращение кольцеобразных М. (сфинктеров) сопровождается сужением или закрытием отверстия. М. радиального направления, наоборот, вызывают при сокращении расширение отверстий. Если М. расположены между костными выступами и кожей, их сокращение обусловливает изменение кожного рельефа. Все скелетные, или соматические (от греч. so'ma - тело), М. по топографо-анатомическому принципу могут быть разделены на М. головы, среди которых различают мимические и жевательные М., воздействующие на нижнюю челюсть, М. шеи, туловища и конечностей. М. туловища покрывают грудную клетку, составляют стенки брюшной полости, вследствие чего их делят на М. груди, живота и спины. Расчленённость скелета конечностей служит основанием для выделения соответствующих групп М.: для верхней конечности - это М. плечевого пояса, плеча, предплечья и кисти; для нижней конечности - М. тазового пояса, бедра, голени, стопы. У человека около 500 М., связанных со скелетом. Среди них одни крупные (например, четырёхглавая М. бедра), другие - мелкие (например, короткие мышцы спины). Совместная работа М. выполняется по принципу синергизма, хотя отдельные функциональные группы М. при выполнении определенных движений работают как антагонисты. Так, спереди на плече находятся двуглавая и плечевая М., выполняющие сгибание предплечья в локтевом суставе, а сзади располагается трёхглавая М. плеча, сокращение которой вызывает противоположное движение - разгибание предплечья. В суставах шаровидной формы происходят простые и сложные движения. Например, в тазобедренном суставе сгибание бедра вызывает пояснично-подвздошная М., разгибание - большая ягодичная. Бедро отводится при сокращении средней и малой ягодичных М., а приводится с помощью пяти М. медиальной группы бедра. По окружности тазобедренного сустава локализуются также М., которые обусловливают вращение бедра внутрь и кнаружи. Наиболее мощные М. размещаются на туловище. Это М. спины - выпрямитель туловища, М. живота, составляющие у человека особую формацию - брюшной пресс . В связи с вертикальным положением тела М. нижней конечности человека стали более сильными, поскольку, кроме участия в локомоции, они обеспечивают опору тела. М. верхней конечности в процессе эволюции, напротив, сделались более ловкими, гарантирующими выполнение быстрых и точных движений. На основе анализа пространственного положения и функциональной деятельности М. современная наука пользуется также следующим их объединением: группа М., осуществляющая движения туловища, головы и шеи; группа М., осуществляющая движения плечевого пояса и свободной верхней конечности; М. нижней конечности. В пределах этих групп выделяются более мелкие ансамбли. В. В. Куприянов. Патология мышц.Нарушения сократительной функции М. и их способности к развитию и поддержанию тонуса наблюдаются при гипертонии, инфаркте миокарда, миодистрофии, атонии матки, кишечника, мочевого пузыря, при различных формах параличей (например, после перенесённого полиомиелита) и др. Патологические изменения функций мышечных органов могут возникать в связи с нарушениями нервной или гуморальной регуляции, повреждениями отдельных М. или их участков (например, при инфаркте миокарда) и, наконец, на клеточном и субклеточном уровнях. При этом может иметь место нарушение обмена веществ (прежде всего ферментной системы регенерации макроэргических соединений - главным образом АТФ) или изменение белкового сократительного субстрата. Указанные изменения могут быть обусловлены недостаточным образованием мышечных белков на почве нарушения синтеза соответствующих информационных, или матричных, РНК, т. е. врождённых дефектов в структуре ДНК хромосомного аппарата клеток. Последняя группа заболеваний, т. о., относится к числу наследственных заболеваний . Саркоплазматические белки скелетных и гладких М. представляют интерес не только с точки зрения возможного участия их в развитии вязкого последействия. Многие из них обладают ферментативной активностью и участвуют в клеточном метаболизме. При повреждении мышечных органов, например при инфаркте миокарда или нарушении проницаемости поверхностных мембран мышечных волокон, ферменты (креатинкиназа, лактатдегидрогеназа, альдолаза, аминотрансферазы и др.) могут выходить в кровь. Т. о., определение активности этих ферментов в плазме крови при ряде заболеваний (инфаркт миокарда, миопатии и др.) представляет серьёзный клинический интерес. Лит.:Энгельгардт В. А., Ферментативные и механические свойства белков мышц, «Успехи современной биологии», 1941, т. 14, в. 2; Сент-Джиордьи А., О мышечной деятельности, пер. с англ., М., 1947; Иванов И. И., Юрьев В. А., Биохимия и патобиохимия мышц, Л., 1961; Поглазов Б. Ф., Структура и функции сократительных белков, М., 1965; Хайаши Т., Как клетки движутся, в кн.: Живая клетка, пер. с англ., 2 изд., М., 1966; Хаксли Г., Механизм мышечного сокращения, в сб.: Молекулы и клетки, пер. с англ., в. 2, М., 1967; Смит Д., Летательные мышцы насекомых, там же; Бендолл Дж., Мышцы, молекулы и движение, пер. с англ., М., 1970; Арронет Н. И., Мышечные и клеточные сократительные (двигательные) модели, Л., 1971; Лёви А., Сикевиц Ф., Структура и функции клетки, пер. с англ., М., 1971; Иванов И. И., Некоторые актуальные проблемы эволюционной биохимии мышц, «Журнал эволюционной биохимии и физиологии» 1972, т. 8, № 3; Gibbons I. R., The biochemistry of motility, «Annual Review of Biochemistry», 1968, v. 37, р. 521. И. И. Иванов. 
Рис. 4. Электронная микрофотография гладкомышечного волокна. Видны актиновые нити (показаны стрелками). 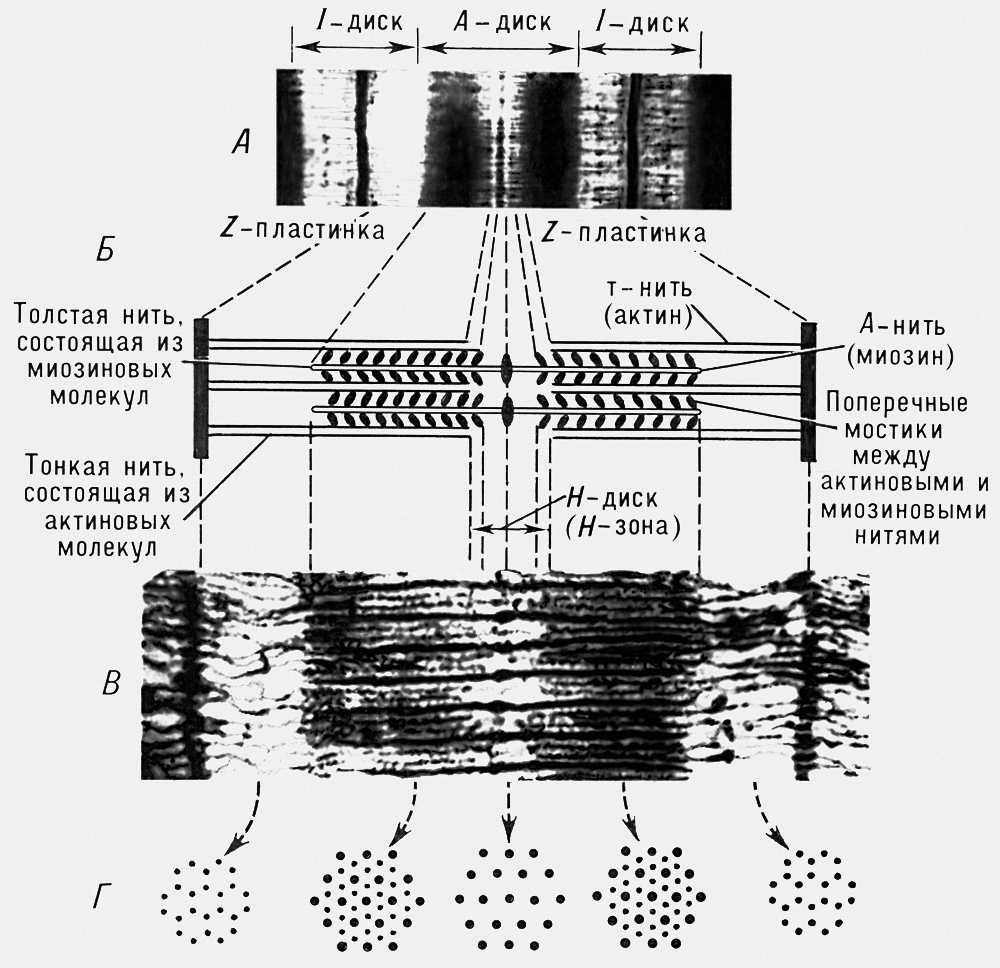
Рис. 3. Строение саркомера поперечнополосатого мышечного волокна: А - электронная микрофотография (малое увеличение), на которой четко видна структура саркомера; Б - схема саркомера; В - электронная микрофотография с высокой разрешающей способностью; Г - поперечное сечение саркомера на различных уровнях, видно положение толстых и тонких нитей в различных участках покоящегося саркомера (по Х. Хаксли). 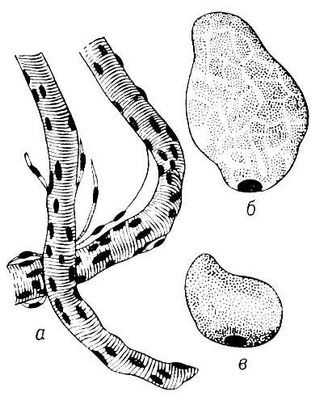
Рис. 1. Поперечнополосатые мышечные волокна человека: а - отрезки двух волокон; б - поперечный разрез волокна, миофибриллы образуют скопления, разграниченные саркоплазмой; в - поперечный разрез волокна с равномерным распределением миофибрилл. 
Рис. 2. Электронная микрофотография саркоплазматической сети и Т-системы мышечного волокна. Мышьяк Мышья'к(лат. Arsenicum), As, химический элемент V группы периодической системы Менделеева, атомный номер 33, атомная масса 74,9216; кристаллы серо-стального цвета. Элемент состоит из одного устойчивого изотопа 75As. Историческая справка. Природные соединения М. с серой (аурипигмент As 2S 3, реальгар As 4S 4) были известны народам древнего мира, которые применяли эти минералы как лекарства и краски. Был известен и продукт обжигания сульфидов М. - оксид М. (III) As 2O 3(«белый М.»). Название arsenikуn встречается уже у Аристотеля; оно произведено от греч. бrsen - сильный, мужественный и служило для обозначения соединений М. (по их сильному действию на организм). Русское название, как полагают, произошло от «мышь» (по применению препаратов М. для истребления мышей и крыс). Получение М. в свободном состоянии приписывают Альберту Великому (около 1250). В 1789 А. Лавуазье включил М. в список химических элементов. Распространение в природе. Среднее содержание М. в земной коре (кларк) 1,7·10 -4% (по массе), в таких количествах он присутствует в большинстве изверженных пород. Поскольку соединения М. летучи при высоких температурах, элемент не накапливается при магматических процессах; он концентрируется, осаждаясь из горячих глубинных вод (вместе с S, Se, Sb, Fe, Co, Ni, Cu и др. элементами). При извержении вулканов М. в виде своих летучих соединений попадает в атмосферу. Так как М. многовалентен, на его миграцию оказывает большое влияние окислительно-восстановительная среда. В окислительных условиях земной поверхности образуются арсенаты (As 5+) и арсениты (As 3+). Это редкие минералы, встречающиеся только на участках месторождений М. Ещё реже встречается самородный М. и минералы As 2+. Из многочисленных минералов М. (около 180) основное промышленное значение имеет лишь арсенопирит FeAsS (см. Мышьяковые руды ). Малые количества М. необходимы для жизни. Однако в районах месторождении М. и деятельности молодых вулканов почвы местами содержат до 1% М., с чем связаны болезни скота, гибель растительности. Накопление М. особенно характерно для ландшафтов степей и пустынь, в почвах которых М. малоподвижен. Во влажном климате М. легко вымывается из почв. В живом веществе в среднем 3·10 -5% М., в реках 3·10 -7%. М., приносимый реками в океан, сравнительно быстро осаждается. В морской воде лишь 1·10 -7% М., но зато в глинах и сланцах 6,6·10 -4%. Осадочные железные руды, железомарганцевые конкреции часто обогащены М. Физические и химические свойства. М. имеет несколько аллотропических модификаций. При обычных условиях наиболее устойчив так называемый металлический, или серый, М. (a-As) - серо-стальная хрупкая кристаллическая масса; в свежем изломе имеет металлический блеск, на воздухе быстро тускнеет, т. к. покрывается тонкой плёнкой As 2O 3. Кристаллическая решётка серого М. ромбоэдрическая ( а= 4,123 Е, угол a = 54°10', х= 0,226), слоистая. Плотность 5,72 г/см 3(при 20°C), удельное электрическое сопротивление 35·10 -8 омЧ м, или 35·10 -6 омЧ см, температурный коэффициент электросопротивления 3,9·10 -3(0°-100 °C), твёрдость по Бринеллю 1470 Мн/м 2, или 147 кгс/мм 2(3-4 по Моосу); М. диамагнитен. Под атмосферным давлением М. возгоняется при 615 °C не плавясь, т. к. тройная точка (см. Диаграмма состояния ) a-As лежит при 816 °C и давлении 36 ат. Пар М. состоит до 800 °C из молекул As 4, выше 1700 °C - только из As 2. При конденсации пара М. на поверхности, охлаждаемой жидким воздухом, образуется жёлтый М. - прозрачные, мягкие как воск кристаллы, плотностью 1,97 г/см 3, похожие по свойствам на белый фосфор . При действии света или при слабом нагревании он переходит в серый М. Известны также стекловидно-аморфные модификации: чёрный М. и бурый М., которые при нагревании выше 270°C превращаются в серый М. Конфигурация внешних электронов атома М. 3 d 104 s 24 p 3. В соединениях М. имеет степени окисления + 5, + 3 и – 3. Серый М. значительно менее активен химически, чем фосфор. При нагревании на воздухе выше 400°C М. горит, образуя As 2O 3. С галогенами М. соединяется непосредственно; при обычных условиях AsF 5- газ; AsF 3, AsCl 3, AsBr 3- бесцветные легко летучие жидкости; AsI 3и As 2l 4- красные кристаллы. При нагревании М. с серой получены сульфиды: оранжево-красный As 4S 4и лимонно-жёлтый As 2S 3. Бледно-жёлтый сульфид As 2S 5осаждается при пропускании H 2S в охлаждаемый льдом раствор мышьяковой кислоты (или её солей) в дымящей соляной кислоте: 2H 3AsO 4+ 5H 2S = As 2S 5+ 8H 2O; около 500°C он разлагается на As 2S 3и серу. Все сульфиды М. нерастворимы в воде и разбавленных кислотах. Сильные окислители (смеси HNO 3+ HCl, HCl + KClO 3) переводят их в смесь H 3AsO 4и H 2SO 4. Сульфид As 2S 3легко растворяется в сульфидах и полисульфидах аммония и щелочных металлов, образуя соли кислот - тиомышьяковистой H 3AsS 3и тиомышьяковой H 3AsS 4. С кислородом М. даёт окислы: оксид М. (III) As 2O 3- мышьяковистый ангидрид и оксид М. (V) As 2O 5- мышьяковый ангидрид. Первый из них образуется при действии кислорода на М. или его сульфиды, например 2As 2S 3+ 9O 2= 2As 2O 3+ 6SO 2. Пары As 2O 3конденсируются в бесцветную стекловидную массу, которая с течением времени становится непрозрачной вследствие образования мелких кристаллов кубической сингонии, плотность 3,865 г/см 3. Плотность пара отвечает формуле As 4O 6: выше 1800°C пар состоит из As 2O 3. В 100 гводы растворяется 2,1 гAs 2O 3(при 25°C). Оксид М. (III) - соединение амфотерное, с преобладанием кислотных свойств. Известны соли (арсениты), отвечающие кислотам ортомышьяковистой H 3AsO 3и метамышьяковистой HAsO 2; сами же кислоты не получены. В воде растворимы только арсениты щелочных металлов и аммония. As 2O 3и арсениты обычно бывают восстановителями (например, As 2O 3+ 2I 2+ 5H 2O = 4HI + 2H 3AsO 4), но могут быть и окислителями (например, As 2O 3+ 3C = 2As + 3CO). Оксид М. (V) получают нагреванием мышьяковой кислоты H 3AsO 4(около 200°C). Он бесцветен, около 500°C разлагается на As 2O 3и O 2. Мышьяковую кислоту получают действием концентрированной HNO 3на As или As 2O 3. Соли мышьяковой кислоты (арсенаты) нерастворимы в воде, за исключением солей щелочных металлов и аммония. Известны соли, отвечающие кислотам ортомышьяковой H 3AsO 4, метамышьяковой HAsO 3, и пиромышьяковой H 4As 2O 7; последние две кислоты в свободном состоянии не получены. При сплавлении с металлами М. по большей части образует соединения ( арсениды ). Получение и применение. М. получают в промышленности нагреванием мышьякового колчедана: FeAsS = FeS + As или (реже) восстановлением As 2O 3углем. Оба процесса ведут в ретортах из огнеупорной глины, соединённых с приёмником для конденсации паров М. Мышьяковистый ангидрид получают окислительным обжигом мышьяковых руд или как побочный продукт обжига полиметаллических руд, почти всегда содержащих М. При окислительном обжиге образуются пары As 2O 3, которые конденсируются в уловительных камерах. Сырой As 2O 3очищают возгонкой при 500-600°C. Очищенный As 2O 3служит для производства М. и его препаратов. Небольшие добавки М. (0,2-1,0% по массе) вводят в свинец, служащий для производства ружейной дроби (М. повышает поверхностное натяжение расплавленного свинца, благодаря чему дробь получает форму, близкую к сферической; М. несколько увеличивает твёрдость свинца). Как частичный заменитель сурьмы М. входит в состав некоторых баббитов и типографских сплавов. Чистый М. не ядовит, но все его соединения, растворимые в воде или могущие перейти в раствор под действием желудочного сока, чрезвычайно ядовиты; особенно опасен мышьяковистый водород . Из применяемых на производстве соединений М. наиболее токсичен мышьяковистый ангидрид. Примесь М. содержат почти все сульфидные руды цветных металлов, а также железный (серный) колчедан. Поэтому при их окислительном обжиге, наряду с сернистым ангидридом SO 2, всегда образуется As 2O 3; большая часть его конденсируется в дымовых каналах, но при отсутствии или малой эффективности очистных сооружений отходящие газы рудообжигательных печей увлекают заметные количества As 2O 3. Чистый М., хотя и не ядовит, но при хранении на воздухе всегда покрывается налётом ядовитого As 2O 3. При отсутствии должной вентиляции крайне опасно травление металлов (железа, цинка) техническими серной или соляной кислотами, содержащими примесь М., т. к. при этом образуется мышьяковистый водород. С. А. Погодин. М. в организме. В качестве микроэлемента М. повсеместно распространён в живой природе. Среднее содержание М. в почвах 4·10 -4%, в золе растений - 3·10 -5%. Содержание М. в морских организмах выше, чем в наземных (в рыбах 0,6-4,7 мгв 1 кгсырого вещества, накапливается в печени). Среднее содержание М. в теле человека 0,08-0,2 мг/кг. В крови М. концентрируется в эритроцитах, где он связывается с молекулой гемоглобина (причём в глобиновой фракции содержится его вдвое больше, чем в геме). Наибольшее количество его (на 1 гткани) обнаруживается в почках и печени. Много М. содержится в лёгких и селезёнке, коже и волосах; сравнительно мало - в спинномозговой жидкости, головном мозге (главным образом гипофизе), половых железах и др. В тканях М. находится в основной белковой фракции, значительно меньше - в кислоторастворимой и лишь незначительная часть его обнаруживается в липидной фракции. М. участвует в окислительно-восстановительных реакциях: окислительном распаде сложных углеводов, брожении, гликолизе и т. п. Соединения М. применяют в биохимии как специфические ингибиторы ферментов для изучения реакций обмена веществ. М. в медицине. Органические соединения М. (аминарсон, миарсенол, новарсенал, осарсол) применяют, главным образом, для лечения сифилиса и протозойных заболеваний. Неорганические препараты М. - натрия арсенит (мышьяковокислый натрий), калия арсенит (мышьяковистокислый калий), мышьяковистый ангидрид As 2O 3, назначают как общеукрепляющие и тонизирующие средства. При местном применении неорганические препараты М. могут вызывать некротизирующий эффект без предшествующего раздражения, отчего этот процесс протекает почти безболезненно; это свойство, которое наиболее выражено у As 2O 3, используют в стоматологии для разрушения пульпы зуба. Неорганические препараты М. применяют также для лечения псориаза. Полученные искусственно радиоактивные изотопы М. 74As (T 1/ 2= 17,5 сут) и 76As (T 1/ 2= 26,8 ч) используют в диагностических и лечебных целях. С их помощью уточняют локализацию опухолей мозга и определяют степень радикальности их удаления. Радиоактивный М. используют иногда при болезнях крови и др. Согласно рекомендациям Международной комиссии по защите от излучений, предельно допустимое содержание 76As в организме 11 мккюри. По санитарным нормам, принятым в СССР, предельно допустимые концентрации 76As в воде и открытых водоёмах 1·10 -7 кюри/л, в воздухе рабочих помещений 5·10 -11 кюри/л. Все препараты М. очень ядовиты. При остром отравлении ими наблюдаются сильные боли в животе, понос, поражение почек; возможны коллапс, судороги. При хроническом отравлении наиболее часты желудочно-кишечные расстройства, катары слизистых оболочек дыхательных путей (фарингит, ларингит, бронхит), поражения кожи (экзантема, меланоз, гиперкератоз), нарушения чувствительности; возможно развитие апластической анемии. При лечении отравлений препаратами М. наибольшее значение придают унитиолу (см. Антидоты ). Меры предупреждения производственных отравлений должны быть направлены прежде всего на механизацию, герметизацию и обеспыливание технологического процесса, на создание эффективной вентиляции и обеспечение рабочих средствами индивидуальной защиты от воздействия пыли. Необходимы регулярные медицинские осмотры работающих. Предварительные медицинские осмотры производят при приёме на работу, а для работающих - раз в полгода. Лит.:Реми Г., Курс неорганической химии, пер. с нем., т. 1, М., 1963, с. 700-712; Погодин С. А., Мышьяк, в кн.: Краткая химическая энциклопедия, т. 3, М., 1964; Вредные вещества в промышленности, под общ. ред. Н. В. Лазарева, 6 изд., ч. 2, Л., 1971. Мышьяк самородный Мышья'к саморо'дный,минерал из класса самородных элементов, химическая формула As: обычны примеси ряда др. элементов: Sb, S, Fe, Ag, Ni; реже Bi и V. Содержание As в М. с. достигает 98%. Кристаллизуется в тригональной системе. Кристаллы - мелкие ромбоэдры псевдокубического габитуса - очень редки. Обычны сплошные зернистые массы в виде скорлуповатых натёков и корок. Цвет оловянно-белый на свежем изломе, чёрный на выветрелой поверхности. Твердость по минералогической шкале 3-3,5; плотность 5630-5800 кг/м 2; хрупок. М. с. в природе обычно образуется из горячих водных растворов. Встречается вместе с минералами Ag, Со, Ni, а также с галенитом, пиритом, антимонитом и др. При выветривании М. с. окисляется и переходит в арсенолит As 2O 3. Крупных скоплений М. с. обычно не образует. Мышьяковая кислота Мышьяко'вая кислота',H 3AsO 4, трёхосновная неорганическая кислота; см. Мышьяк . Мышьяковистый водород Мышьякови'стый водоро'д,арсин, AsH 3, бесцветный газ без запаха (примеси обычно вызывают чесночный запах), t kип- 62,4°C, t пл- 113,5°C. Открыт в 1775 К. В. Шееле . Чистый М. в. получают действием воды на арсенид натрия Na 3As. При восстановлении растворимых в кислотах соединений мышьяка водородом в момент выделения образуется смесь М. в. с водородом, например: As 2O 3+ 6Zn + 6H 2SO 4= 2AsH 3+ 6ZnSO 4+ 3H 2O. Если эту смесь пропускать через стеклянную трубку, нагретую до 400-500°C М. в. разлагается на водород и мышьяк, который образует на холодных частях трубки чёрный налёт с зеркальным блеском; описанный способ служит для обнаружения мышьяка. Эту пробу разработал в 1836 английский химик Дж. Марш (J. Marsh, 1794-1846). М. в. - один из наиболее токсичных промышленных ядов. Отравления носят преимущественно острый характер, протекают тяжело. По характеру действия на организм М. в. - яд с преобладающим гемолитическим (кроверазрушающим) действием. Скрытый период от 2 до 8 ч; к концу его появляются головная боль, головокружение, озноб, рвота и боли в животе. Кожа приобретает окраску, напоминающую загар. Температура тела вначале повышена до 38-39°C. Через некоторое время может развиться кома. Профилактика: применение металлов и кислот, не загрязнённых мышьяком; механизация производственных процессов; герметизация аппаратуры, рациональная эффективная вентиляция. Мышьяковые руды Мышьяко'вые ру'ды,природные минеральные образования, содержание As в которых достаточно для экономически целесообразного извлечения мышьяка и его соединений. Известно свыше 120 минералов, содержащих As. Наиболее распространённые минералы М. р.: арсенопирит (мышьяковый колчедан) FeAsS с содержанием As 46,0%; мышьяковистый колчедан (лёллингит) FeAs 2(72,8% As); реальгар AsS (70,1% As); аурипигмент As 2S 3(61,0% As). Большинство месторождений М. р. относится к эндогенной серии, плутоногенному и вулканогенному классам гидротермальной группы. Соединения As чаще всего встречаются в комплексе с цветными и благородными металлами (Cu, Zn, Pb, Au, Ag и др.). As в таких рудах содержится как в форме независимых минералов, так и в виде изоморфной примеси в составе сульфидов и др. соединений. По промышленной классификации месторождения М. р. подразделяются на несколько типов: мышьяковые (арсенопиритовые и реальгаро-аурипигментные), золотомышьяковые, полиметаллическо-мышьяковые, медно-мышьяковые, мышьяково-кобальтовые, мышьяково-оловянные. Максимальное содержание As в промышленных рудах составляет 2%, но обычно разрабатываются более богатые руды с содержанием 5-10%; более бедные руды обогащают гравитационными методами и флотацией . Месторождения М. р. известны в СССР. За рубежом наиболее значительные месторождения имеются в США (Бьютт, Голд-Хилл и др.), Швеции (Булиден), Мексике (Матеуала, Чиуауа), Японии (Кашиока, Сасачатани), Боливии (Потоси) и др. странах. См. также Мышьяк . В. И. Смирнов. Мышьяковый колчедан Мышьяко'вый колчеда'н,минерал, сульфоарсенид железа; см. Арсенопирит . Мышьякорганические соединения Мышьякоргани'ческие соедине'ния,органические соединения, содержащие атом мышьяка, непосредственно связанный с атомом углерода. Важнейшие типы М. с., содержащих трёхвалентный мышьяк: первичные RAsH 2, вторичные R 2AsH и третичные R 3As арсины; галогенарсины RAsX 2и RaAsX (X - атом галогена); окиси и кислоты RAsO, RAs(OH) 2, R 2As(OH); диарсины, например тетраметилдиарсин (дикакодил) (CH 3) 2As-As (CH 3) 2; полиарсины (-RAs-) х;арсенобензолы Ar-As = As-Ar. Из соединений пятивалентного мышьяка известны галогениды R nAsX 5-n, производные мышьяковых кислот типа RAsO(OH) 2, R2AsO(OH), R 3AsO и R 4AsOH, а также пентафенилмышьяк (C 6H 5) 5As. Особый класс составляют илиды мышьяка Ar 3As +-`CR 2. Иногда неправильно к М. с. относят эфиры мышьяковистой и мышьяковой кислот (RO) 3As и (RO) 3AsO, не содержащие связи As - С. Методы получения М. с. разнообразны. Наиболее важные: 1. Действие металлоорганических соединений на галогениды мышьяка: 3RMgX + AsX 3® R 3As + 3MgX 2. 2. Действие алкилирующих агентов на соли мышьяковистой кислоты (реакция Майера): CH 3I + (NaO) 3As ® CH 3As(O)(ONa) 2+ Nal. 3. Конденсация галогенидов мышьяка с ароматическими или непредельными соединениями:
4. Взаимодействие солей диазония с солями мышьяковистой кислоты (реакция Барта): C 6H 5N 2 +X -+ (NaO) 3As ® C 6H 5As(O) (ONa) 2+ NaX + N 2. 5. Взаимодействие солей арилазокарбоновых кислот с галогенидами мышьяка ( Несмеянова реакция ). Многие М. с. - физиологически активные вещества. Так, открытый в 1909 П. Эрлихом сальварсан стал первым синтетическим химиотерапевтическим препаратом. Он успешно применялся для лечения сифилиса. Такие М. с., как адамсит и люизит , были предложены в 1-ю мировую войну 1914-18 как отравляющие вещества. Мыэнги Мыэ'нги,мыонги, народ, живущий в предгорьях Аннамских гор в центральных и южных районах ДРВ. Численность около 500 тыс. чел. (1970, оценка). По происхождению и языку близки вьетнамцам, от которых отличаются рядом черт в материальной культуре (бамбуковые дома на сваях, женская сшивная юбка и др.). Религия М. - культ предков и вера в различных духов. Основное занятие - рисосеяние. 1, 2, 3, 4 |
|||||||
