 |
|
Популярные авторы:: БСЭ :: Борхес Хорхе Луис :: Горький Максим :: Раззаков Федор :: Херберт Фрэнк :: Чехов Антон Павлович :: Грин Александр :: Толстой Лев Николаевич :: Азимов Айзек :: Астафьев Виктор Петрович Популярные книги:: Дюна (Книги 1-3) :: The Boarding House :: Преодоление :: Три цвета времени :: Упражнения по стилистике русского языка :: Талисман из Рэдволла :: Рассказы, очерки, фельетоны :: Закрой рот, джинн – кишки простудишь… :: Андропов. 7 тайн генсека с Лубянки :: Нет прощения! |
Большая Советская Энциклопедия (ИМ)ModernLib.Net / Энциклопедии / БСЭ / Большая Советская Энциклопедия (ИМ) - Чтение (стр. 4)
Клетки одного типа (В-клетки) происходят из костного мозга и при встрече с антигеном превращаются в клетки, образующие антитела (плазматические клетки). Клетки другого типа (Т-клетки) происходят из тимуса. Им свойственна способность специфически реагировать на антигенные молекулы и обеспечивать взаимодействие В-клеток с антигеном.
В иммунологически зрелом (иммунокомпетентном) организме фагоцитирующие клетки и Т- и В-лимфоциты осуществляют все формы специфического ответа: образуют циркулирующие антитела, относящиеся к разным классам (верхняя часть рис. 2), реализуют иммунные реакции клеточного типа — замедленную повышенную чувствительность, отторжение трансплантата и др. Так организм отвечает на ряд бактериальных и паразитарных инвазий (туберкулёз, бруцеллёз, лейшманиоз), а также на пересадку клеток и тканей от другого организма (см. , ). Дифференцировка и взаимодействие этих клеток под влиянием антигена могут привести к возникновению иммунологической «памяти» или специфической иммунологической толерантности. Сравнительная И. изучает иммунный ответ у разных видов животных. Эволюционное толкование явлений иммунитета помогает выяснить их механизмы. Лимфоидная система и способность к образованию специфических антител впервые появляются только у позвоночных. Например, морская минога имеет примитивный лимфоэпителиальный тимус, лимфоидные островки в селезёнке и костном мозге и циркулирующие лимфоциты; у неё образуются антитела и возникает иммунологическая память, но ассортимент антигенов, на которые отвечает минога, очень ограничен. У примитивных хрящевых рыб (акул, скатов) лимфоидная система более развита; они способны реагировать на большее число антигенов. Типичные плазматические клетки появляются у хрящевых, лучепёрых и костистых рыб. У этих животных вырабатывается несколько типов иммуноглобулинов. У земноводных впервые в филогенетическом ряду образуется система плазматических клеток, синтезирующих высоко- и низкомолекулярные иммуноглобулины, различающиеся по антигенным свойствам. Весьма похожая система имеется у пресмыкающихся. Система (состоящая из различных белков нативной сыворотки), по-видимому, очень древняя, так как в сходной форме имеется как у низших, так и у высших позвоночных. У большинства млекопитающих иммунные реакции развиваются в полной мере только после рождения. Во время эмбрионального развития, когда зародыш защищен от действия антигенов, функционирует система избирательного переноса иммуноглобулинов от матери к плоду. Однако к 4—5 месяцам плод человека самостоятельно образует иммуноглобулины М и G. Птицы и млекопитающие, в том числе человек, обладают одинаковым спектром иммунологических реакций. Степень иммунореактивности связана с возрастом и заметно снижается по мере старения организма. Физиология иммунных реакций изучает механизмы, с помощью которых организм обнаруживает и удаляет «чужое» — вещества, не являющиеся нормальными компонентами его собственных тканей: мёртвые и злокачественно перерожденные клетки, собственные поврежденные молекулы, чужеродные клетки и молекулы, бактерии, вирусы, простейшие, гельминты и их яды и т. п. Функциональным выражением чужеродности антигена является его способность вызывать образование специфических антител и соединяться с ними. Природа антигенности, вопрос о том, почему организм, не вырабатывая антитела на громадное множество собственных молекул, образует антитела к бесконечному числу чужеродных антигенов, сущность специфического иммунного ответа, в частности синтеза антител, являются главными вопросами так называемой теории образования антител. Предполагают, что образование антител, т. е. биосинтез высокоспециализированных белковых молекул, осуществляется подобно синтезу других белков плазмы крови (см. ). Общая теория иммунологических реакций должна объяснить физико-химическую природу антигенности, описать молекулярные механизмы синтеза антител и расшифровать иммунохимическую специфичность. Создание такой теории возможно при последовательном решении трёх важнейших и взаимосвязанных проблем иммунного ответа: 1) генетические основы разнообразия иммуноглобулинов; 2) вопросы о том, сколько различных по специфичности антител может синтезировать клетка, о межклеточных взаимодействиях и о том, на каком уровне, клеточном или субклеточном, осуществляется действие антигена; 3) механизм специфической иммунологической толерантности (отсутствие специфического ответа на антиген). Первая попытка химической интерпретации иммунологических реакций была предпринята П. Эрлихом (1900). Он полагал, что каждая антителообразующая клетка обладает преформированной «боковой цепью», случайно пространственно соответствующей антигену. «Боковые цепи», отделившиеся от клетки-носителя и попавшие в кровоток, отождествлялись с антителами. Эта гипотеза поразительно близка к современным представлениям о биосинтезе тем, что в ней предполагается предсуществование (до воздействия антигена) для каждого вида антител. Антигенные молекулы должны только «выбрать» (произвести селекцию) предсуществующую структуру и усилить её воспроизведение. Популярность селекционной идеи Эрлиха была поколеблена открытием К. Ландштейнера (1936), который показал, что большое количество искусственных антигенов, полученных синтетическим путём, может вызвать образование специфических антител. В связи с этим американские учёные Ф. Брейнль и Ф. Гауровиц, Д. Александер и С. Мадд (1930) предположили, что преформированных антител не существует. Антиген вмешивается в процесс образования молекулы глобулина, нарушая её сборку. В результате образуется антитело со специфичной для данного антигена структурой. Действие антигена в этом случае является инструктивным, что легко объясняет беспредельное разнообразие синтезируемых организмом антител. Американский учёный Л. Полинг (1940) приписывал антигену роль «матрицы», на которой складываются полипептидные цепи антитела. Новым этапом в развитии И. было появление концепции австралийских учёных Ф. Бёрнета и Ф. Феннера (1941), рассматривавших синтез антител как частный случай адаптивного белкового синтеза, подобный синтезу у бактерий. Предполагалось, что антиген в клетке осуществляет косвенное инструктивное действие, вызывая изменения в комплексе ферментов, участвующих в синтезе молекулы антитела. Впоследствии эта концепция была дополнена гипотезой о существовании особых «меток» для собственных антигенов организма, что объясняло естественную толерантность к ним. Согласно представлению американских учёных Р. Швита и Р. Оуэна (1957), антиген, подобно , вызывает соответствующие изменения дезоксирибонуклеиновой кислоты (ДНК), следствием которых является биосинтез молекул антител. Американский учёный Д. Голдштейн (1960) предположил аналогичное действие антигена на информационную рибонуклеиновую кислоту (и-РНК). В 1950 немецкий учёный Н. Ерне выдвинул новую гипотезу специфического иммунного ответа, основанную на селекционной идее Эрлиха. Гипотеза «натуральной селекции» Ерне сводилась к тому, что в эмбриональном периоде в тимусе образуются различные по специфичности молекулы антител. Комплекс антигена с соответствующим антителом попадает в синтезирующую антитела клетку, которая использует антитело как модель для образования подобных молекул. Ерне постулировал отсутствие антител к собственным антигенам организма и «распознавание» только чужеродных конфигураций. Дальнейшим развитием селекционной идеи была клонально-селекционная теория приобретённого иммунитета, выдвинутая Ф. Бёрнетом (1957). Клоном называют группу клеток, происшедших путём деления от одной клетки-предшественницы. По Бёрнету, лимфоидная система иммунологически зрелого организма содержит множество (не менее 10 4—10 5) клонов клеток, способных специфически отвечать на различные антигены. Природа генетического разнообразия иммуноглобулинов неизвестна. Однако именно клонально-селекционная теория представляется наиболее правдоподобной и соответствующей современным представлениям о биосинтезе белка. Отсутствие реакции на собственные антигены Бёрнет объяснил устранением «запрещенных клонов» (способных синтезировать антитела к «своему») в эмбриональном периоде. Согласно этой теории, антиген, попадая в организм, «выбирает» клетку, которая способна образовать соответствующее антитело, и стимулирует её к размножению с последующим синтезом антитела. Как происходит этот выбор — на уровне клеточных клонов (как полагает Бёрнет) или субклеточных единиц, — зависит от того, сколько различных по специфичности молекул антител способна синтезировать клетка. Можно думать, что клетка несёт генетическую информацию для синтеза более чем 10 5различных иммуноглобулинов. Однако в результате дифференцировки её способность синтезировать антитела практически подавлена. Антиген вызывает дерепрессию синтеза соответствующих антител, в результате чего синтезируются антитела только одной специфичности. Это положение лежит в основе гипотезы «репрессии-депрессии», выдвинутой американским учёным Л. Силардом, австралийским — И. Финчем и советским учёными В. П. Эфроимсоном, А. Е. Гурвичем и Р. С. Незлиным. Физиология иммунных реакций изучает также факторы, регулирующие количественные характеристики иммунного ответа, в том числе роль нервной системы (преимущественно гипоталамуса), гормонов, возраста, питания, состояния организма (в частности, степени утомления) и внешних воздействий. Теперь известно, что не только гормоны гипофиза и надпочечников могут изменять иммунологическую реактивность, но и плацента выделяет особый гормон, который в значительной степени тормозит иммунные реакции организма матери на антигены плода. Иммунопатология изучает не только чрезмерные или повреждающие организм иммунные реакции (см. ), но и заболевания, сопровождающиеся дефектами иммунной системы: наследственные и приобретённые агаммаглобулинемии и иммуноглобулинопатии при опухолях лимфо-ретикулярной ткани, при нефрозах, после применения цитостатических лекарственных препаратов и после облучения. В иммунопатологии особое внимание уделяется методам торможения и стимуляции иммунного ответа. Усиление иммунного ответа неспецифическими стимуляторами (так называемыми адъювантами) или трансплантацией активных лимфоидных тканей перспективно при инфекционных заболеваниях и при дефектах иммунной системы. И наоборот, торможение иммунного ответа — лечебный приём при заболеваниях с чрезмерной или нежелательной активностью иммунной системы. Торможения достигают, повреждая лимфоидные клетки облучением, азотистыми ипритами, антиметаболитами, кортикостероидными гормонами, антилимфоцитарной сывороткой. Иммунный ответ подавляют также пассивным введением антител, например введением матери антирезусных антител для предотвращения гемолитической желтухи новорождённых. В последние годы интенсивно изучаются реакции организма на клетки и макромолекулы индивидуумов того же или другого вида. Эту отрасль называют неинфекционной И. Каждый многоклеточный организм обладает некоторыми уникальными, неповторимыми особенностями строения белков и клеточных мембран. Отличие одного индивидуума от другого обусловлено генетическими механизмами. Именно по этой причине введённые в организм извне клетки и молекулы распознаются как чужеродные и вызывают комплекс иммунных реакций, направленных на их удаление. Поэтому, несмотря на самую совершенную хирургическую технику, пересаженные органы и ткани обычно отторгаются, будучи не в состоянии преодолеть барьер тканевой несовместимости; её изучением занимается трансплантационная И. Другой раздел неинфекционной И. — иммунология опухолей — изучает опухолевые антигены и механизмы распознавания и удаления злокачественно перерожденных клеток. В круг проблем неинфекционной И. входит также разработка способов создания специфической иммунологической толерантности, которые в будущем позволят сделать трансплантацию органов практически применяемым методом лечения всевозможных заболеваний. Получаемые И. данные служат основой для развития прикладной, клинической И. и таких её основных направлений, как , , . Иммунологические методы исследования широко используются для тонкого анализа в разнообразных отраслях медицины (гематологии, акушерстве, дерматологии и пр.) и биологии (в биохимии, эмбриологии, генетике и антропологии). Проблемами И. в СССР занимаются более 50 научно-исследовательских учреждений. Крупнейшие из них — институт эпидемиологии и микробиологии им. Н. Ф. Гамалеи АМН СССР (Отдел иммунологии и онкологии этого института — международный центр по опухолеспецифическим антигенам), Московский институт вакцин и сывороток им. И. И. Мечникова, Государственный контрольный институт медико-биологических препаратов им. Л. А. Тарасовича, Московский институт эпидемиологии и микробиологии, Ленинградский институт экспериментальной медицины. За рубежом вопросами И. занимаются: Институт иммунологии (Базель) и Институт биохимии Лозаннского университета (Швейцария), Национальный институт медицинских исследований (Милл-Хилл, Великобритания), Национальный институт рака, Национальный институт здравоохранения, а также Рокфеллеровский институт медицинских исследований (США). Научно-исследовательский институт иммунологии (Прага, Чехословакия), Институт Л. Пастера (Париж, Франция) и др. С 1963 Всемирная организация здравоохранения (ВОЗ), осуществляя свою программу по И., создаёт справочные центры по иммунологии и иммуноглобулинам, созывает симпозиумы и совещания по иммунопатологии, иммунологии паразитарных заболеваний, иммунотерапии рака, по типированию антигенов тканевой несовместимости, по клеточному иммунитету. В СССР работы по И. публикуются в ряде медицинских и биологических журналов: «Журнал микробиологии, эпидемиологии и иммунобиологии» (с 1924); «Патологическая физиология и экспериментальная терапия» (с 1957); «Вопросы вирусологии» (с 1956); «Медицинская паразитология и паразитарные болезни» (с 1923); «Бюллетень экспериментальной биологии и медицины» (с 1936). За рубежом ряд периодических изданий целиком посвящен проблемам И.: «Journal of Immunology» (Balt., с 1916); «Journal of Experimental Medicine» (N. Y., с 1896); «Journal of Allergy» (St. Louis, с 1929); «Immunology» (Oxf., с 1958); «Clinical and Experimental Immunology» (Oxf., с 1966); «Immunochemistry» (N. Y., с 1964); «Advances in Immunology» (N. Y. — L., с 1961); «Zeitschrift fьr Immunitдts- und Allergieforschung» (Jena — Stuttg., с 1909); «International Archives of Allergy and Applied Immunology» (N. Y. — Basel, с 1950); «Revue d'Immunologie et de Thйrapie antimicrobienne» (P., с 1935). Вопросам И. посвящены многие статьи в «Бюллетене Всемирной организации здравоохранения» (с 1964), издаваемом на русском языке, и отдельные выпуски из серии технических докладов ВОЗ, а также статьи в международном «Журнале гигиены, эпидемиологии, микробиологии и иммунологии», издаваемом на русском языке в Праге (с 1957). Лит.:Незлин Р. С., Биохимия антител, М., 1966; Фонталин Л. Н., Иммунологическая реактивность лимфоидных органов и клеток, Л., 1967; Петров Р. В., Введение в неинфекционную иммунологию, Новосиб., 1968; Здродовский П. Ф., Проблемы инфекции, иммунитета и аллергии, 3 изд., М., 1969; Эфроимсон В. П., Введение в медицинскую генетику, 2 изд., М., 1968; его же, Иммуногенетика, М., 1971; Бойд У. К., Основы иммунологии, пер. с англ., М., 1969; Бернет Ф. М., Клеточная иммунология, пер. с англ., М., 1971, с. 11; Pressman D., Grossberg A. L., The structural basis of antibody specificity, N. Y. — Amst., 1968; Humphrey J. Н., White R. G., Immunology for students of medicine, 3 ed., Oxf., 1970. А. Н. Мац. Практическая, в том числе и клиническая, И. занимается использованием иммунологических реакций в целях диагностики, профилактики и лечения ряда заболеваний. Она тесно связана с медицинской и ветеринарной микробиологией, а также с эпидемиологией, физиологией и патофизиологией, биохимией, эндокринологией и др. Самостоятельными разделами практической И. является вирусная И., И. паразитарных заболеваний. И. изучает антигенный состав микроорганизмов, особенности иммунных процессов при различных видах инфекций и неспецифические формы устойчивости организма к инфекционному возбудителю. Всё большее значение приобретают изучение иммунологических процессов и иммунологической перестройки организма, вызванных неинфекционными антигенами экзогенного и эндогенного происхождения, разработке методов борьбы с аллергическими заболеваниями (см. , ). Интенсивно развиваются и другие разделы клинической И.: радиационная И., изучающая нарушения иммунологической реактивности организма под влиянием облучения; иммуногематология, исследующая антигенный состав клеток крови, причины и механизм развития иммунологических поражений системы крови и др. И. разрабатывает методы иммунопрофилактики, иммунотерапии и иммунодиагностики. Клиническая И. использует различные методы исследования. Так, при изучении природы и свойств антигенов и антител используется биохимические и физико-химические методы. С помощью изотопных индикаторов и флюоресцентной микроскопии изучают судьбу антигенов в организме и закономерности антителообразования на клеточном уровне. Механизмы развития неспецифических воспалительных и аллергических реакций исследуют биохимическими и цитохимическими методами. Иммунологические методы исследования основаны на специфичности взаимодействия антигена (микроба, вируса, чужеродного белка и пр.) с антителами. Раздел И., изучающий реакции антигена с антителами сыворотки крови, называется . К наиболее распространённым иммунологическим методам относятся: реакция преципитации, реакция агглютинации, реакция лизиса, реакция нейтрализации. Широкое распространение получает изучение взаимодействия антигена с иммунными клетками. Многие методы И. обладают очень высокой специфической чувствительностью (например, реакция превосходит по чувствительности методы аналитической химии) и используются в других дисциплинах, например в судебной медицине. В СССР и за рубежом И. преподают в медицинских и ветеринарных вузах на кафедрах патологической физиологии, микробиологии, общей патологии, а также в спец. научно-исследовательских институтах. Вопросы клинической И. обсуждаются на международных конгрессах по микробиологии и аллергологии и освещаются во многих отечественных и зарубежных журналах. Лит.:Доссе Ж., Иммуногематология, пер. с франц., М., 1959; Радиационная иммунология, М., 1965; Лабораторные методы исследования в неинфекционной иммунологии, под ред. О. Е. Вязова, М., 1967; Иоффе В. И., Клиническая и эпидемиологическая иммунология, [Л., 1968]; Практическая иммунология, под ред. П. Н. Бургасова и И. С. Безденежных, М., 1969. А. Х. Канчурин, Н. В. Медуницын. 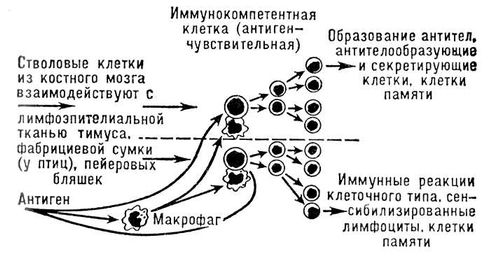 
Иммунопатология
|
|||||||

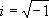 — мнимая единица. Разделяя комплексный И. а. на вещественную и мнимую части, получают активную
R
aи реактивную
X
aсоставляющие И. а. — активное и реактивное акустические сопротивления. Первое связано с трением и потерями энергии на излучение звука акустической системой, а второе — с реакцией сил инерции (масс) или сил упругости (гибкости). Реактивное сопротивление в соответствии с этим бывает инерционное или упругое.
— мнимая единица. Разделяя комплексный И. а. на вещественную и мнимую части, получают активную
R
aи реактивную
X
aсоставляющие И. а. — активное и реактивное акустические сопротивления. Первое связано с трением и потерями энергии на излучение звука акустической системой, а второе — с реакцией сил инерции (масс) или сил упругости (гибкости). Реактивное сопротивление в соответствии с этим бывает инерционное или упругое.